


 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
 .意大利罗马大学的Fulvio Cacace教授受白磷分子结构的启发又合成了和白磷分子极具类似的N4分子.已知断裂1mol N-N键需吸收167kJ的能量,生成1mol N≡N键放出942kJ的能量.判断下列说法正确的是( )
.意大利罗马大学的Fulvio Cacace教授受白磷分子结构的启发又合成了和白磷分子极具类似的N4分子.已知断裂1mol N-N键需吸收167kJ的能量,生成1mol N≡N键放出942kJ的能量.判断下列说法正确的是( )| A、N4转化为N2的过程是一个放热过程 |
| B、N4的沸点比P4(白磷)的高 |
| C、N4与N2互为同分异构体 |
| D、N4晶体属于原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
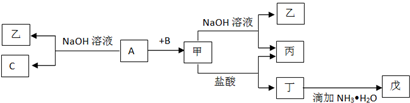
 图中,A为空气中常见的气体单质,B、C、E是金属单质,D为非金属单质.已知:
图中,A为空气中常见的气体单质,B、C、E是金属单质,D为非金属单质.已知:| 高温 |
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2+ |
| B、Ba2+ |
| C、C1- |
| D、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量的A1分别与足量的盐酸、烧碱反应转移的电子数 |
| B、36gH2O和1.204×1024个O2在标准状况下所占体积 |
| C、pH相等的氨水与醋酸钠溶液中由水电离出的OH-浓度 |
| D、pH相等的H2SO4和CH3COOH稀释相同倍数之后溶液的pH值 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解质溶液呈电中性,胶体带电荷 |
| B、溶液中溶质粒子的运动有规律,而胶体粒子的运动无规律 |
| C、溶液中溶质粒子一定不带电,胶体中分散质粒子带有电荷,且通电后溶质粒子分别向两极移动,胶体粒子向某一极移动 |
| D、溶液中通过一束光线时无特殊现象,胶体中通过一束光线时有明显的光带 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com