
�������巨������Cr2O72���ķ�ˮ��ԭ�����£���Cr2O72�������Է�ˮ�м���FeSO4��7H2O����Cr2O72����ԭΪCr3����������Һ��pH��ʹ������Ԫ��ת��Ϊ����൱��FeII [FeIIIx��CrIII2-x]O4 (�������塢�������ֱ�ʾԪ�صļ�̬���ij�����������1 mol Cr2O72���ķ�ˮ������Ҫ����a mol FeSO4��7H2O�����н�����ȷ���� �� ��
A��x=0��5��a��8 B��x��0��5��a��10
C��x��1��5��a��8 D��x��1��5��a��10
 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2- 7 |
2- 7 |
2- 7 |
2- 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1������ˮ�����۸���![]() ���ڣ���д������������������������ԭ
���ڣ���д������������������������ԭ![]() �����ӷ�Ӧ����ʽ����ƽ��_______________________��
�����ӷ�Ӧ����ʽ����ƽ��_______________________��
��2���ɣ�1���Ľ����ȷ������������x=__________��
��3���ݣ�2���Ľ��������ˮ��Cr(��)��CrO3�ƣ�������FeSO4��7H2O��CrO3��������ӦΪ���ٲ��ܳ�ȥ��ˮ�е�Cr(��), ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
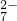 �ķ�ˮ��ԭ�����£���Cr2O
�ķ�ˮ��ԭ�����£���Cr2O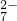 �����Է�ˮ�м���FeSO4?7H2O����Cr2O
�����Է�ˮ�м���FeSO4?7H2O����Cr2O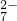 ��ԭΪCr3+��������Һ��pH��ʹ������Ԫ��ת��Ϊ����൱��Fe��[Fe��x?Cr��2-x]O4���������塢�������ֱ�ʾԪ�صļ�̬���ij�����������1mol Cr2O
��ԭΪCr3+��������Һ��pH��ʹ������Ԫ��ת��Ϊ����൱��Fe��[Fe��x?Cr��2-x]O4���������塢�������ֱ�ʾԪ�صļ�̬���ij�����������1mol Cr2O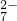 �ķ�ˮ������Ҫ����a mol FeSO4?7H2O�����н�����ȷ����
�ķ�ˮ������Ҫ����a mol FeSO4?7H2O�����н�����ȷ�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com