
����Ŀ����.ij�¶��£���ˮ�е�c(H+)=2.0��10-7mol��L-1�����ʱ��Һ��c(OH-)=____ mol��L-1������ˮ��____(����������������������)�ԣ����¶Ȳ��䣬����ϡ����ʹc(H+)=5.0��10-6 mol��L-1����c(OH-)=__ mol��L-1��
��. (1)��2mL 0.1mol��L-1��NaCl��Һ�У�����2mL 0.1mol��L-1��AgNO3��Һ���ɹ۲쵽____���˷�Ӧ�����ӷ���ʽΪ______________�� ���˻��Һ���ˣ���������2mL 0.1mol��L-1��KI��Һ�����裬�ɹ۲쵽_______________�� ��Ӧ�����ӷ���ʽΪ____________��
(2)����˵������ȷ����___��
A.��ϡ����ϴ��AgCl��������ˮϴ�����AgClС
B.�������ʵ��ܽⶼ�����ȵ�
C. ������Ӧ�г��ӹ����ij���������Ŀ����ʹ������ȫ
D.��ȥ��Һ�е�Mg2+����OH-����Mg2+��![]() ��Ч���ã�˵�� Mg(OH)2���ܽ�ȱ�MgCO3��
��Ч���ã�˵�� Mg(OH)2���ܽ�ȱ�MgCO3��
��. 25 �棬���ֳ�����ĵ��볣�����±���ʾ��
Ka1 | Ka2 | |
H2SO3 | 1.3��10-2 | 6.3��10-8 |
H2CO3 | 4.2��10-7 | 5.6��10-11 |
(1)![]() �ĵ��볣������ʽ K =_____________��
�ĵ��볣������ʽ K =_____________��
(2)H2SO3��Һ��NaHCO3��Һ��Ӧ����Ҫ���ӷ���ʽΪ______________��
���𰸡�2.0��10-7 �� 8��10-9 ��ɫ���� Ag++Cl-=AgCl�� ��ɫ������Ϊ��ɫ���� AgCl(s)+I-(aq)![]() AgI(s)+Cl-(aq) BD
AgI(s)+Cl-(aq) BD ![]()
![]()
��������
����������ʵĵ���ƽ��ԭ����ƽ�ⳣ������ʽ������ؼ��㣻���ݳ����ܽ�ƽ�⼰����ת�������жϷ�Ӧ������д������ӷ���ʽ�������ܶȻ��������ܽ�ȵĹ�ϵ�������
��.��ˮ��ˮ�����������Ũ�ȵ���������Ũ�ȣ�����c(H+)=2.0��10-7mol��L-1ʱ����Һ��c(OH-)=c(H+)=2.0��10-7mol��L-1����ʱ��Һ�����ԣ�����ƽ�ⳣ��K=c(OH-)c(H+)=2.0��10-7 ��2.0��10-7=4.0��10-14������ϡ����ʹc(H+)=5.0��10-6mol��L-1����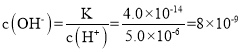 ��
��
��. (1)��Ӧ�����Ȼ����������ƣ��۲쵽��ɫ���������ӷ�ӦΪAg++Cl-=AgCl����AgCl�м���2mL 0.1mol/L��KI��Һ����������ת��������AgI���۲쵽��ɫ����ת��Ϊ��ɫ���������ӷ�ӦΪAgCl(s)+I-(aq) AgI(s)+Cl-(aq)��
(2)A.�Ȼ��������ܽ�ƽ���д����ܶȻ�������Ksp=c(Ag+)c(Cl)��������Ũ������ƽ�������������У���ϡ����ϴ��AgCl��������ˮϴ�����AgClС����A��ȷ��
B.���ʵ��ܽ�ȴ����¶ȵ����߶����ӣ������ʵ��ܽ������ȵģ���Щ�����ܽ�����¶�����С����Щ�����ܽ�ʱ���ȵģ���B����
C. Ϊʹ������ȫ��������������ij���������ʹ���ӳ�����ȫ����C��ȷ��
D. Mg(OH)2���ܽ�ȱ�MgCO3С����D����
�ʴ�ΪBD��
��. (1)HSO3�ĵ��뷽��ʽΪ��HSO3H++SO32-��ƽ�ⳣ������ʽΪK=![]() ��
��
(2)�ɱ���֪H2SO3�Ķ�������С��H2CO3��һ�����룬��������ǿ��H2SO3>H2CO3>HSO3-�����Է�Ӧ����Ҫ���ӷ���ʽΪH2SO3+HCO3=HSO3+CO2��+H2O��


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�ˮ�����ӻ�ԼΪ1��10��12����VaL pH��2��������Һ��VbL pH��11��NaOH��Һ��ϣ��������Һ��pH��10�������(Va��Vb) L����Va��VbΪ ( )
A. 2��11B. 2��9C. 11��2D. 9��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ����(����)
A.��K2S��Һ�м�ˮϡ��![]() ���С
���С
B.����������Һ�еμ�ϡ����õ���pH=5�Ļ����Һ��:c(Na+)<c(NO3-)
C.ȡc(H+)=0.01mol��L-1������ʹ����1L���ֱ����0.3gп��������ͬ�����³�ַ�Ӧ,������п��Ӧ��ƽ�����ʴ�
D.��CuS��FeS�����͵Ļ����Һ�м�������Na2S���壬![]() ���ֲ���
���ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܼ��еĵ���ʵ�������е�H��ת�Ƹ��ܼ����ӣ���HCl��H2O=H3O++Cl-����֪H2SO4��HNO3�ڱ������еĵ���ƽ�ⳣ���ֱ�ΪKal(H2SO4)=6.3��10-9��Ka(HNO3)=4.2��10-10������˵����ȷ����( )
A.H2SO4�ڱ������еĵ��뷽��ʽΪH2SO4+2CH3COOH=SO42-+2CH3COOH2+
B.H2SO4�ڱ������У�![]() ��c(HSO4-)+2c(SO42-)+c(CH3COO-)
��c(HSO4-)+2c(SO42-)+c(CH3COO-)
C.Ũ�Ⱦ�Ϊ0.1mol��L-1��H2SO4��HNO3�ı�������Һ��pH(H2SO4)>pH(HNO3)
D.��HNO3�ı�������Һ�м�������ᣬ ��ֵ��С
��ֵ��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����ʯ��Ϊԭ���Ʊ�ijЩ������Ʒ�IJ������̡���ش�

��1��д����Ӧ�ڵĻ�ѧ����ʽ________________��
��2��B������������B�Ľṹ��ʽΪ___________________��
��3����Ӧ�ٺ͢۵�����������______________��______________��
��4��д����Ӧ�ܻ�ѧ����ʽ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���Ҳ���Ҫ��ɫ�Լ�ƿ������Լ���
A. ������ B. Ũ���� C. Ũ���� D. ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɺ����ˮ��ȡ����ص�һ�ֹ������£�
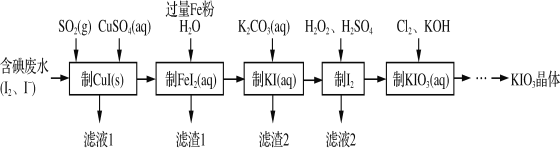
�� д��KIO3���ճ������е�һ����ҪӦ��________________________��
�� �����������ˮ�����Ƿ��е���I2�ij����Լ���________(д�Լ�����)��
�� ͨ��SO2��Ŀ���ǽ�I2��ԭΪI�����÷�Ӧ�����ӷ���ʽΪ______________________��
�� �������������ʵ��Ʊ���Ӧ�У����漰������ԭ��Ӧ�IJ����ǡ���________����
�� ����KI(aq)��ʱ�����¶���ˮ�����ӻ�ΪKw��1.0��10��13��Ksp[Fe(OH)2]��9.0��10��15��
Ϊ����0.9 mol��L��1 FeI2��Һ��Fe2+ˮ�����ɽ�״������I-����ʼ����K2CO3���뱣����Һ��pH������______��
�� ����KIO3��Һ����Ӧ�����ӷ���ʽΪ__________________��

�� KCl��KIO3���ܽ��������ͼ��ʾ������������KIO3(aq)���õ�KIO3����IJ�������Ϊ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.����������Һ��pHֵ��25 ����������д��������̣���20mL0.01 mol��L��1 KOH��Һ��30mL0.005mol��L��1H2SO4��Һ��ϲ���ˮ��100ml��
��1����KOH��Һ��pHֵ_______________��
��2����H2SO4��Һ��pHֵ_______________��
��3������Һ��pHֵ_______________��
II.��10�����ijǿ����Һ��1�����ijǿ����Һ��Ϻ���Һ�����ԣ�����֮ǰ����ǿ���pH���ᣩ��ǿ���pH���֮��Ӧ����Ĺ�ϵ__________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com