
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-═CaCO3↓ Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 | |
| D. | H++OH-═H2O Ba(OH)2+H2SO4═BaSO4↓+2H2O |
分析 A.该离子反应为可溶性铜盐和强碱溶液的反应,且不能生成其它沉淀;
B.该离子反应为可溶性碳酸钠和强酸的反应;
C.该离子方程式为可溶性钙盐或氢氧化钙与可溶性碳酸盐的反应且不生成其它沉淀;
D.该离子反应为强酸、强碱中和反应且不生成其它沉淀或气体.
解答 解:A.该离子反应为可溶性铜盐和强碱溶液的反应,且不能生成其它沉淀,化学方程式如CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,故A错误;
B.该离子反应为可溶性碳酸钠和强酸的反应,化学方程式如Na2CO3+2HCl═2NaCl+CO2↑+H2O,故B错误;
C.该离子方程式为可溶性钙盐或氢氧化钙与可溶性碳酸盐的反应且不生成其它沉淀,碳酸钠和硝酸钙都是可溶性强电解质,且二者反应不生成其它沉淀或气体、弱电解质等,故C正确;
D.该离子反应为强酸、强碱中和反应且不生成其它沉淀或气体,化学方程式如:HCl+NaOH=NaCl+H2O,故D错误;
故选C.
点评 本题考查离子方程式与化学方程式关系,为高频考点,明确物质性质及离子方程式书写规则是解本题关键,侧重考查学生发散思维能力及分析判断能力,易错选项是A.


科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,100g 17%H2O2水溶液中含氧原子总数为NA | |
| B. | 常温常压下,2.8g N2气体分子中所含的共用电子对数目为0.3NA | |
| C. | 0.2mol/L的NaCl溶液中含有的Cl-数是0.2NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
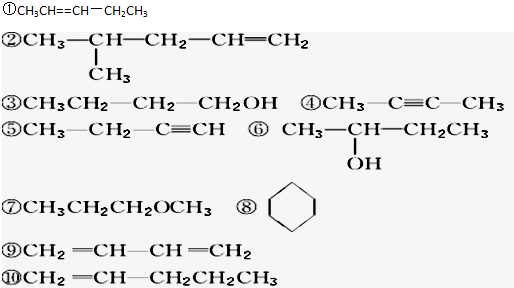
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打--Na2CO3 | B. | 熟石灰--Ca (OH)2 | C. | 漂白粉-Ca(ClO)2 | D. | 氯水--Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
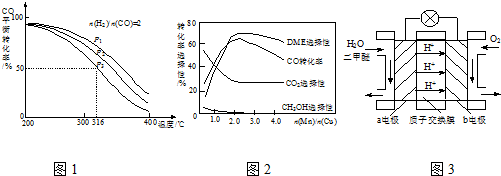
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>③>①=② | B. | ①=②>③>④ | C. | ②>①>③>④ | D. | ④>③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
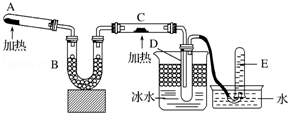 化学是一门以实验为基础的自然科学.
化学是一门以实验为基础的自然科学.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com