
【题目】TiO2在光照射下可使水分解:2H2O![]() 2H2↑+O2↑,该过程类似植物的光合作用。下图是光照射下TiO2分解水的装置示意图。下列叙述正确的是( )
2H2↑+O2↑,该过程类似植物的光合作用。下图是光照射下TiO2分解水的装置示意图。下列叙述正确的是( )

A. 该装置将光能只转化为电能
B. TiO2电极上发生的反应为:2H++2e-===H2↑
C. 该装置工作时,电流由TiO2电极经R流向铂电极
D. 该装置工作时,TiO2电极附近溶液的pH变小
科目:高中化学 来源: 题型:
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4· H 2O(三盐),主要制备流程如下。

(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
(2)将滤液I、滤液III合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物( Mr=322) ,其化学式为______________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为_____________;滤液II中溶质的主要成分为________(填化学式)。
(4)步骤⑥合成三盐的化学方程式为____________ 。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得某碳氢化合物A中含碳80%,含氢20%,该化合物的实验式是__________,又测得该化合物的相对分子质量是30,该化合物的分子式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C、D四种元素,原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素。试回答下列有关的问题:
(1)写出D元素价电子的电子排布式:______________。
(2)D可形成化合物[D(H2O)6](NO3)3 。
①[D(H2O)6](NO3)3中阴离子的立体构型是_____________。NO3-中心原子的轨道杂化类型为__________。
②在[D(H2O)6] 3+中D3+与H2O之间形成的化学键称为______,1 mol [D(H2O)6] 3+ 中含有的σ键有________mol。
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中________(填化学式)为非极性分子。另一种物质的电子式为_____________。
(4)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为A、C形成化合物的晶胞结构图以及晶胞的剖面图:

晶胞中距离一个A+最近的C-有________个,这些C-围成的图形是______________,若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则A+的离子半径为________cm(用含NA与ρ的式子表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物F是治疗感冒药的主要成分之一,其合成路线如下:

已知:
① (R、R'、R"均代表烃基;X代表卤素原子);
(R、R'、R"均代表烃基;X代表卤素原子);
②A蒸气的密度是相同条件下氢气密度的53倍。
请回答下列问题:
(1)D中官能团的名称为______。
(2)E的结构简式为____________。
(3)写出反应②的化学方程式:___________________。
(4)B的消去反应产物可以用于合成高分子化合物G,G的结构简式是________;若G的平均相对分子质量为9000,则其平均聚合度约为___________(保留整数)。
(5)符合下列条件的C的同分异构体有________种(考虑顺反异构)
①能与氢氧化钠溶液反应 ②分子中含有两种官能团。
任写一种存在顺反异构的同分异构体的结构简式__________(写反式结构);
(6)C的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同_____(填字母序号)。
A.核磁共振仪 B.元素分析仪 C.质谱仪 D.红外光谱仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属钠的叙述正确的是( )
A. 金属钠可以保存在煤油中
B. 金属钠着火时,可用水来灭火
C. 钠与硫酸铜溶液反应可置换出铜
D. 实验时用剩的钠块不能放回原试剂瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸吸收塔排出的尾气需要处理才能排放到大气中,其处理方法为:先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。
为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果:
铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
请计算:
(1)该铵盐中氮元素的质量分数是____%。
(2)若铵盐质量为15.00g,浓硫酸增加的质量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2Cl2是广泛用于橡胶工业的硫化剂,常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体,其结构与H2O2类似。下列说法错误的是( )
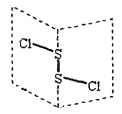
A. S2Cl2分子中的两个S原子均是sp3杂化
B. S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
C. S2Br2与S2Cl2结构相似,熔沸点S2Br2>S2Cl2
D. S2Cl2分子中的S为+1价,是含有极性键和非极性键的非极性分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com