
【题目】下列热化学方程式中,正确的是
A.已知:![]()
![]() ,则1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于
,则1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于![]() kJ
kJ
B.![]() 、30MPa下,将
、30MPa下,将![]() mol
mol![]() 和
和![]() mol
mol![]() 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成![]() 放热
放热![]()
![]() 其热化学方程式为:
其热化学方程式为:![]()
![]()
C.![]()
![]() ,则
,则![]()
D.在101kPa时,2g![]() 完全燃烧生成液态水,放出
完全燃烧生成液态水,放出![]() kJ热量,氢气燃烧的热化学方程式表示为
kJ热量,氢气燃烧的热化学方程式表示为![]()
![]()
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G、H是相对分子质量依次增大的气体,它们均由短周期元素组成,具有如下性质:
①B能使湿润的红色石蕊试纸变蓝,A、C、D不能使湿润的石蕊试纸变色,E、G均可使湿润的蓝色石蕊试纸变红;
②F呈红棕色;
③G和H均能使品红褪色,A在H中安静燃烧并产生苍白色火焰;
④C在D中完全燃烧生成E和H2O,同时放出大量热,工业上可利用该反应焊接或切割金属。
请回答下列问题:
(1)E的电子式为_____,D中所含元素的基态原子核外电子排布式为___,C分子中的σ键和π键的个数之比为___。
(2)写出实验室用固体药品制取B的化学方程式_______________。
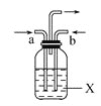
(3)若从a口通入气体G,从b口通入气体F,X为氯化钡溶液,观察到的现象是_____________,
反应的离子方程式为_________________。
(4)已知:E(g)+3A(g)![]() CH3OH(l)+H2O(l) ΔH=-53.66 kJ·mol-1
CH3OH(l)+H2O(l) ΔH=-53.66 kJ·mol-1
2CH3OH(l)![]() CH3OCH3(g)+H2O(l) ΔH=-23.4 kJ·mol-1
CH3OCH3(g)+H2O(l) ΔH=-23.4 kJ·mol-1
写出E有催化剂时与A合成二甲醚(CH3OCH3)的热化学方程式_____________。
(5)气体C能使硫酸酸化的高锰酸钾溶液褪色,产物之一是E,该反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸甲酯是一种无色透明油状液体,相对分子质量为152,密度为1.184gcm﹣3,沸点223.3℃,熔点﹣86℃,微溶于水,易溶于有机溶剂,露置在空气中则易缓慢变色。由水杨酸和甲醇在浓硫酸存在条件下反应制得水杨酸甲酯(冬青油)的反应如下:

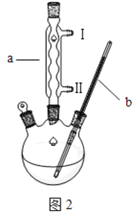
某学校的实验探究小组利用如图装置制备冬青油.步骤如下
①将三颈烧瓶、量筒,置于烘箱中干燥10min;
②用天平称取6.9g水杨酸,用量筒分别量取30mL(约24g)甲醇,6mL浓硫酸,然后将3种试剂分别加入已干燥的三颈烧瓶中,组装好实验装置后置于磁力搅拌加热器上加热;
③加热到85~95℃,反应结束后将盛有混合物的烧瓶置于冷水浴中冷却,然后再将冷却后的混合物倒入分液漏斗中,依次加入NaHCO3溶液和30mL水,充分震荡,静置,分层;
④弃去水层,将有机层注入干燥的锥形瓶中,加入适量无水氯化钙;
⑤将步骤④所得的产品蒸馏,收集221~224℃的馏分,称得产物质量为4.56g
试回答下列问题:
(1)装置中仪器a的作用是_______________;水应该从________(填“Ⅰ”或“Ⅱ”)处流入,仪器b的适宜规格为___________(填序号);
①10℃ ②50℃ ③150℃
(2)加入NaHCO3溶液的目的除了将冬青油中的甲醇、水杨酸、硫酸等除去外,还有___________;加入水震荡分层后,冬青油的粗产品在_______(填“上”或“下”)层;
(3)在本实验分离过程中,水层应该从分液漏斗的_________________(填“上口倒出”或“下口放出”);
(4)本次实验冬青油的产率是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
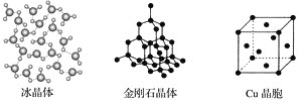
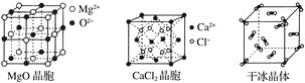
【题目】如图为几种晶体或晶胞的示意图:
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是____。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:___。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能___(填“大于”或“小于”)MgO晶体,原因是____。
(4)每个Cu晶胞中实际占有___个Cu原子,CaCl2晶体中Ca2+的配位数为__。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学术语或表示方法不正确的是
A. S2-的结构示意图: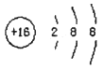
B. CO2的结构式:O=C=O
C. 醋酸的分子式:CH3COOH
D. 乙烯的结构简式:CH2=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及有机物的性质或应用的说法不正确的是![]()
A.淀粉、纤维素、蛋白质都是天然高分子化合物
B.用于奥运“祥云”火炬的丙烷是一种清洁燃料
C.乙酸和油脂都能与氢氧化钠溶液反应
D.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为以惰性电极进行电解:
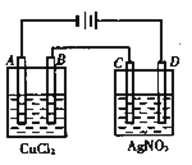
(1)写出A 、B、C、D各电极上的电极反应式和总反应方程式:A:_______________,B:_____________,C:_______________,D:_____________,
(2)电解AgNO3溶液的总反应化学方程式:________;
(3)在A、B、C、D各电极上析出生成物的物质的量比_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种金属组成的合金10g投入足量的稀硫酸中,反应完全后得到氢气11.2L(标准状况下),此合金可能是 ( )
A.镁铝合金B.镁铁合金C.铝铁合金D.镁锌合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素的基态价电子排布式为_____________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______________,提供孤电子对的成键原子是_____________。
②氨的沸点_________(填“高于”或“低于”)膦(PH3),原因是__________________;氨是_________分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______________键形成的晶体。
(4)某镍白铜合金的立方晶胞结构如图所示。
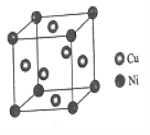
①晶胞中铜原子与镍原子的数量比为___________。
②若合金的密度为dg/cm3,晶胞边长a=______________nm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com