
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2 molA和1 mol B,发生反应:2A(g)+B(g)![]() 2D(g) △H=QkJ·mol-1。相关条件和数据见下表:
2D(g) △H=QkJ·mol-1。相关条件和数据见下表:
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/1C | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是( )
A. 实验Ⅲ达平衡后,恒温下再向容器中通入lmolA和1molD,平衡不移动
B. 升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C. 实验Ⅲ达平衡后容器内的压强是实验Ⅰ的![]() 倍
倍
D. K3>K2>K1
【答案】A
【解析】A.实验III中,
2A(g)+B(g)![]() 2D(g)
2D(g)
起始(mol/L) 1 0.5 0
反应 0.5 0.25 0.5
平衡 0.5 0.25 0.5
化学平衡常数为K=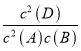 =
=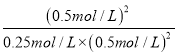 =4L/mol,温度不变,平衡常数不变,实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molD,则此时容器中c(A)=1mol/L,c(B)=0.25mol/L,c(D)=1mol/L,此时浓度商Qc=
=4L/mol,温度不变,平衡常数不变,实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molD,则此时容器中c(A)=1mol/L,c(B)=0.25mol/L,c(D)=1mol/L,此时浓度商Qc=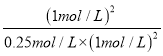 =4L/mol=K,平衡不发生移动,故A正确;B.升高温度,增大了分子的能量,增加了活化分子百分数,使反应速率加快,但反应的活化能不变,故B错误;C.根据理想气体状态方程pV=nRT,反应起始时向容器中充入2molA和1molB,实验III达平衡时,n(D)=1mol,根据反应方程式,则平衡时n(A)=1mol,n(B)=0.5mol,实验I达平衡时,n(D)=1.5mol,根据反应方程式,n(A)=0.5mol,n(B)=0.25mol,则实验III达平衡后容器内的压强与实验I达平衡后容器内的压强之比为
=4L/mol=K,平衡不发生移动,故A正确;B.升高温度,增大了分子的能量,增加了活化分子百分数,使反应速率加快,但反应的活化能不变,故B错误;C.根据理想气体状态方程pV=nRT,反应起始时向容器中充入2molA和1molB,实验III达平衡时,n(D)=1mol,根据反应方程式,则平衡时n(A)=1mol,n(B)=0.5mol,实验I达平衡时,n(D)=1.5mol,根据反应方程式,n(A)=0.5mol,n(B)=0.25mol,则实验III达平衡后容器内的压强与实验I达平衡后容器内的压强之比为![]() =
=![]() =
=![]() ≠
≠![]() ,故C错误;D.反应为2A(g)+B(g)2D(g),比较实验I和III,温度升高,平衡时D的量减少,化学平衡向逆反应方向移动,则K3<K1,温度相同,平衡常数相同,则K1=K2,综上,则平衡常数的关系为:K3<K2=K1,故D错误;故选A。
,故C错误;D.反应为2A(g)+B(g)2D(g),比较实验I和III,温度升高,平衡时D的量减少,化学平衡向逆反应方向移动,则K3<K1,温度相同,平衡常数相同,则K1=K2,综上,则平衡常数的关系为:K3<K2=K1,故D错误;故选A。


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z原子序数依次减小,它们原子的最外层电子数之和为14.X与Z同主族,Y与W同主族,且Y的原子半径大于Z.下列叙述正确的是( )
A.原子半径:W>X>Y
B.X的单质不能与Z的氧化物反应
C.W的单质在Y的单质中燃烧产生淡蓝色火焰
D.X、Y可形成既有离子键又有共价键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用食用白醋(醋酸浓度约1 molL-1)进行下列实验,能证明醋酸为弱电解质的是( )
A.白醋中滴入石蕊试液呈红色 B.白醋加入豆浆中有沉淀产生
C.蛋壳浸泡在白醋中有气体放出 D.pH试纸显示白醋的pH为2~3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有等体积等物质的量浓度的氢硫酸和亚硫酸各两份,分别各通入氯气和氧气。下图中绘的是溶液的pH(y)与通入气体的量(x)的关系图线,其中能正确代表反应中pH变化的图线为( )(注:酸性氢硫酸<亚硫酸)

A. a(为氢硫酸中通入氯气) B. b(为亚硫酸中通入氧气)
C. c(为氢硫酸中通入氧气) D. d (为亚硫酸中通入氯气)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知①2C(s)+O2(g)===2CO(g) △H=-221.0kJ·mol-1
②2H2(g)+O2(g)===2H2O(g) △H= -483.6kJ·mol-1
则反应C(s)+H2O(g)===CO(g)+H2(g)的△H为 ( )
A. +131.3kJ·mol-1B. -131.3kJ·mol-1
C. -352.3kJ·mol-1D. +262.6kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com