
| A、1.6 mol |
| B、2.8 mol |
| C、3.2 mol |
| D、3.6 mol |
科目:高中化学 来源: 题型:
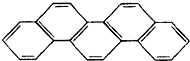 有一种有机物,因其酷似奥林匹克旗中的五环(如图),科学家称其为奥林匹克烃,下列有关奥林匹克烃的说法正确的是( )
有一种有机物,因其酷似奥林匹克旗中的五环(如图),科学家称其为奥林匹克烃,下列有关奥林匹克烃的说法正确的是( )| A、该烃属于烯烃 |
| B、该烃分子中只含非极性键 |
| C、该烃的二氯代物只有一种 |
| D、该烃完全燃烧生成H2O的物质的量小于CO2的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X2+2Y2═2XY2 |
| B、2X2+Y2═2X2Y |
| C、3X2+Y2═2X3Y |
| D、X2+3Y2═2XY3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
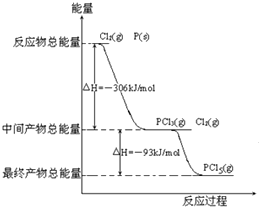 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如下图所示(图中的△H表示生成1mol产物的数据). 根据上图回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如下图所示(图中的△H表示生成1mol产物的数据). 根据上图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应①的反应热为221kJ |
| B、碳的燃烧热为△H=-221kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为△H=-57.3kJ/mol |
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-2.92 kJ?mol-1 |
| B、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-18 kJ?mol-1 |
| C、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-73 kJ?mol-1 |
| D、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-0.72 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
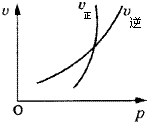
| A、N2O3(g)?NO2(g)+NO(g); 恒容时加入N2O3,平衡正向移动 |
| B、N2(g)+3H2(g)?2NH3(g); 将氨气液化分离后,有利于加快正反应速率 |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g); 加大氧气浓度,能提高氨气平衡转化率 |
| D、2SO2(g)+O2(g)?2SO3(g); 增大压强,平衡常数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com