
”¾ĢāÄæ”æČēĻĀĮłøöĶ¼ÖŠ£¬ŗį×ų±źĪŖijČÜŅŗÖŠ¼ÓČėijĪļÖŹµÄĪļÖŹµÄĮæ£¬×Ż×ų±źĪŖÉś³É³ĮµķµÄĪļÖŹµÄĮ棬½«Ķ¼ÖŠµÄ×ÖÄø“śŗÅĢīČėĻĀ±ķ”£

ČÜŅŗ | ¼ÓČėµÄĪļÖŹ | ×ÖÄø“śŗÅ |
¢Ł±„ŗĶŹÆ»ŅĖ® | ĶعżĮæCO2 | ________ |
¢ŚAlCl3ČÜŅŗ | ĶعżĮæNH3 | ________ |
¢ŪMgCl2”¢AlCl3»ģŗĻČÜŅŗ | ÖšµĪ¼ÓNaOHČÜŅŗÖĮ¹żĮæ | ________ |
¢ÜAlCl3ČÜŅŗ | ÖšµĪ¼ÓNaOHČÜŅŗÖĮ¹żĮæ | ________ |
¢Żŗ¬ÉŁĮæHClµÄAlCl3ČÜŅŗ | ÖšµĪ¼ÓNaOHČÜŅŗÖĮ¹żĮæ | ________ |
”¾“š°ø”æB C A E F
”¾½āĪö”æ
ŹŌĢā¢Ł±„ŗĶŹÆ»ŅĖ®ĶعżĮæCO2ĘųĢ壬ӦĻČÓŠ³Įµķ£ŗCa£ØOH£©2+CO2=CaCO3”ż+H2O£¬ŗóĶØČėÓėĒ°Ņ»²½µČĮæµÄCO2ĘųĢ壬³ĮµķČܽāCaCO3+CO2+H2O=Ca£ØHCO3£©2£¬¶ŌÕÕĶ¼ĻńÓ¦ĪŖB£»¢Ś°±Ė®ŹĒČõ¼ī£¬²»ÄÜČܽāĒāŃõ»ÆĀĮ£¬ĀČ»ÆĀĮČÜŅŗ¼ÓČė¹żĮæ°±Ė®µÄ·“Ó¦·½³ĢŹ½ĪŖ£ŗAlCl3+3NH3H2OØTAl£ØOH£©3”ż+3NH4Cl£¬¶ŌÕÕĶ¼ĻńÓ¦ĪŖC£»¢ŪMgCl2”¢AlCl3µÄ»ģŗĻŅŗ£¬ÖšµĪ¼ÓČėNaOHČÜŅŗÖĮ¹żĮ棬ĻČŹĒÉś³ÉĒāŃõ»ÆĆ¾ŗĶĒāŃõ»ÆĀĮ³Įµķ£¬MgCl2+2NaOHØTMg£ØOH£©2”ż+2NaCl£»AlCl3+3NaOHØTAl£ØOH£©3”ż+3NaCl£¬ŗóŹĒĒāŃõ»ÆĀĮČܽā£¬Al£ØOH£©3+NaOHØTNaAlO2+2H2O£¬Mg£ØOH£©2²»ČÜ£¬¶ŌÕÕĶ¼ĻńÓ¦ĪŖA£®¢ÜĀČ»ÆĀĮČÜŅŗ£¬¼ÓČėĒāŃõ»ÆÄĘ£¬ĒāŃõ»ÆÄĘŗĶĀČ»ÆĀĮÖ®¼ä·“Ó¦Öš½„²śÉś³ĮµķÖ±µ½³ĮµķĮæ×ī“ó£¬AlCl3+3NaOHØTAl£ØOH£©3”ż+3NaCl£¬ŗóŹĒĒāŃõ»ÆĀĮČܽā£¬Al£ØOH£©3+NaOHØTNaAlO2+2H2O£¬¶ŌÕÕĶ¼ĻńÓ¦ĪŖE£»¢Żŗ¬ÉŁĮæHClµÄĀČ»ÆĀĮČÜŅŗ£¬¼ÓČėĒāŃõ»ÆÄĘ£¬ĻČŹĒŗĶŃĪĖįÖ®¼ä·¢ÉśÖŠŗĶ·“Ӧɜ³ÉĀČ»ÆÄĘŗĶĖ®£¬Ć»ÓŠ³Įµķ£¬HCl+NaOH=NaCl+H2O£¬Č»ŗóĒāŃõ»ÆÄĘŗĶĀČ»ÆĀĮÖ®¼ä·“Ó¦Öš½„²śÉś³ĮµķÖ±µ½³ĮµķĮæ×ī“ó£¬AlCl3+3NaOHØTAl£ØOH£©3”ż+3NaCl£¬ŗóŹĒĒāŃõ»ÆĀĮČܽā£¬Al£ØOH£©3+NaOHØTNaAlO2+2H2O£¬¶ŌÕÕĶ¼ĻńÓ¦ĪŖF£»¹ŹĢī£ŗB£»C£»A£»E£»F£»


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪŽÉ«ĶøĆ÷µÄ¼īŠŌČÜŅŗÖŠ£¬ÄÜ“óĮæ¹²“ęµÄĄė×Ó×éŹĒ£Ø £©
A.Na+”¢H+”¢SO42©”¢HCO3©
B.Cu2+”¢K+”¢SO42©”¢NO3©
C.Na+”¢K+”¢Cl©”¢NO3©
D.Mg2+”¢K+”¢SO42©”¢Cl©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē»ÆѧŌŚČÕ³£Éś»īÖŠÓĆĶ¾¹ć·ŗ£¬Ķ¼¼×ŹĒĆ¾-“ĪĀČĖįÄĘČ¼ĮĻµē³Ų£¬µē³Ų×Ü·“Ó¦ĪŖMg+ClO-+H2O=Cl-+Mg(OH)2”ż£¬Ķ¼ŅŅŹĒŗ¬Cr2O72-µÄ¹¤Ņµ·ĻĖ®µÄ“¦Ąķ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. Ķ¼¼×ÖŠ·¢ÉśµÄ»¹Ō·“Ó¦ŹĒMg2++ClO-+H2O+2e-=Cl-+Mg(OH)2”ż
B. Ķ¼ŅŅÖŠCr2O72-Ļņ¶čŠŌµē¼«ŅĘ¶Æ£¬ÓėøĆ¼«ø½½üµÄOH-½įŗĻ£¬×Ŗ»Æ³ÉCr(OH)3³żČ„
C. Ķ¼ŅŅµē½ā³ŲÖŠ£¬ČōÓŠ0.84 gŃō¼«²ÄĮĻ²ĪÓė·“Ó¦£¬ŌņŅõ¼«»įÓŠ168 mL£Ø±ź×¼×“æö£©µÄĘųĢå²śÉś
D. ČōĶ¼¼×Č¼ĮĻµē³ŲĻūŗÄ0.36 gĆ¾²śÉśµÄµēĮæÓĆŅŌĶ¼ŅŅ·ĻĖ®“¦Ąķ£¬ĄķĀŪÉĻæɲśÉś1.07gĒāŃõ»ÆĢś³Įµķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°Ń4molAŗĶ2.5molB»ģŗĻÓŚ2LĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ3A(g)+2B(s)![]() xC(g)+D(g)£¬5minŗó·“Ó¦“ļµ½Ę½ŗā£¬ČŻĘ÷ÄŚŃ¹Ēæ±äŠ”£¬²āµĆDµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.05mol”¤L-1”¤min-1£¬“ķĪóµÄŹĒ
xC(g)+D(g)£¬5minŗó·“Ó¦“ļµ½Ę½ŗā£¬ČŻĘ÷ÄŚŃ¹Ēæ±äŠ”£¬²āµĆDµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.05mol”¤L-1”¤min-1£¬“ķĪóµÄŹĒ
A. AµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.15mol”¤L-1”¤min-1 B. Ę½ŗāŹ±£¬CµÄÅضČĪŖ0.25 mol”¤L-1
C. BµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.1mol”¤L-1”¤min-1 D. Ę½ŗāŹ±£¬ČŻĘ÷ÄŚŃ¹ĒæĪŖŌĄ“µÄ0.875±¶
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬a”¢b”¢c”¢d¾łĪŖŹÆÄ«µē¼«£¬Ķصē½ųŠŠµē½ā£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(”” ””)
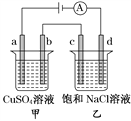
A. µēĀ·ÖŠµē×ÓĮ÷Ļņ£ŗøŗ¼«”śd”śc”śb”śa”śÕż¼«
B. a”¢cĮ½¼«²śÉśĘųĢåµÄĪļÖŹµÄĮæĻąµČ
C. SO42-Ļņbµē¼«ŌĖ¶Æ£¬Cl-Ļņcµē¼«ŌĖ¶Æ
D. ĶصēŗóŅŅÉÕ±µĪČė·ÓĢŖČÜŅŗd¼«»į±äŗģ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠA”¢B”¢C”¢DĖÄÖÖ»ÆŗĻĪļ£¬ĘäŃęÉ«·“Ó¦µÄ»šŃę¾łĪŖ»ĘÉ«”£ĘäÖŠCŹĒŅ»ÖÖµ»ĘÉ«¹ĢĢ壬¼ÓČČ¹ĢĢåAæÉÉś³ÉD£¬Ķ¬Ź±µĆµ½ÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒµÄĪŽÉ«ĘųĢ唣AÓėBČÜŅŗ»ģŗĻŗóæɵƵ½D”£
£Ø1£©Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½£ŗA”¢_______£»B”¢_______£»C”¢_______£»D”¢_______”£
£Ø2£©Š“³öAÓėB·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_________________________________________”£
£Ø3£©ŌŚ¼×”¢ŅŅ”¢±ū”¢¶”ĖÄøöÉÕ±ÖŠø÷¼ÓČė100 mLĖ®£¬ŌŁ·Ö±š¼ÓČė0.1 mol µÄĻĀĮŠĪļÖŹ£ŗ¢ŁÄĘ”¢¢ŚŃõ»ÆÄĘ”¢¢Ū¹żŃõ»ÆÄĘ”¢¢ÜĒāŃõ»ÆÄĘ£¬¹ĢĢåĶźČ«Čܽāŗó£¬ĖÄøöÉÕ±ÖŠČÜÖŹµÄÖŹĮæ·ÖŹżÓɓ󵽊”µÄĖ³ŠņŹĒ£ØĢī±ąŗÅ£©___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ£»ÆѧŠĖȤŠ”×éÓĆČēĶ¼ĖłŹ¾¹ż³Ģ³żČ„AlCl3ÖŠŗ¬ÓŠµÄMg2+”¢K+ŌÓÖŹĄė×Ó²¢¾”æÉÄܼõÉŁAlCl3µÄĖšŹ§”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
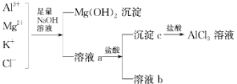
(1)Š“³ö»ģŗĻĪļÖŠ¼ÓČė×ćĮæĒāŃõ»ÆÄĘČÜŅŗŹ±£¬ČÜŅŗÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_______________________”£
(2)ĒāŃõ»ÆÄĘČÜŅŗÄÜ·ńÓĆ°±Ė®“śĢę£¬ĪŖŹ²Ć“£æ___________________________”£
(3)ČÜŅŗaÖŠ“ęŌŚµÄĄė×ÓÓŠ________________£»ŌŚČÜŅŗaÖŠ¼ÓČėŃĪĖįŹ±ŠčæŲÖĘŃĪĖįµÄĮ棬ĪŖŹ²Ć“£æ__________________________________”£ĪŖ“Ė£¬øĽų·½·ØŹĒ___________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø£©
A. ±ź×¼×“æöĻĀ£¬l molČĪŗĪĪļÖŹµÄĢå»ż¾łĪŖ22.4 L
B. CH4µÄĦ¶ūÖŹĮæĪŖ16 g
C. 1mol H2OµÄÖŹĮæĪŖ18 gmol£1
D. 1 mol”¤L£1NaClČÜŅŗµÄŗ¬ŅåŹĒ1 LČÜŅŗÖŠŗ¬ÓŠ58.5 g NaCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠČĖÉč¼ĘĮĖČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆĄ“Ģ½¾æÄĘÓėĖ®·“Ó¦(Ģś¼ÜĢصČŅĒĘ÷ŅŃĀŌ)”£ŹµŃéĒ°ŌŚĻš½ŗČūĻĀ¶Ė“ņŅ»øöŠ”æ×ŃØ£¬½«Ņ»“󊔏ŹÖŠµÄÄĘæé¹Ģ¶ØÓŚÕėĶ·ĻĀ¶Ė£¬ĻņÉĻ³é¶ÆÕėĶ·Ź¹ÄĘæé²ŲÓŚæ×ŃØÄŚ”£ŌŚ²£Į§·“Ó¦¹ÜČװČėŹŹĮæĖ®(Ź¹ÄĘæé²»ÓėĖ®½Ó“„)”£ŹµŃ鏱£¬°ĪČ„Ļš½ŗČéĶ·£¬°“×”Ļš½ŗČū£¬½«ÕėĶ·»ŗ»ŗĻņÉĻ°ĪĘš£¬Ź¹ÄĘÓėĖ®½Ó“„£¬·“Ó¦¹ÜÄŚµÄŅŗĢå±»²śÉśµÄĘųĢåŃ¹³ö£¬Į÷ČėÖĆÓŚĻĀ·½µÄÉÕ±ÖŠ£¬ĘųĢåŌņ±»ŹÕ¼ÆŌŚ·“Ó¦¹ÜÄŚ”£
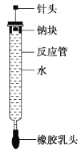
(1)ÄĘÓėĖ®·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ__________________________________________________”£
(2)ŹµŃéÖŠ”°ÄĘæéČŪ»ÆĪŖÉĮĮĮµÄŠ”Ēņ”±ĖµĆ÷_____________________£»ĻņÉÕ±ÖŠµÄČÜŅŗÖŠµĪ¼Ó____________£¬ČÜŅŗ±äŗģ£¬ĖµĆ÷ÄĘÓėĖ®·“Ӧɜ³É¼īŠŌĪļÖŹ”£
(3)Čē¹ūŹµŃéĒ°¼ÓČė·“Ó¦¹ÜÄŚĖ®µÄĢå»żĪŖa mL£¬ÓūŹ¹Ė®×īÖÕČ«²æ±»Åųö£¬ŌņĖłČ”½šŹōÄʵÄÖŹĮæÖĮÉŁĪŖ____________g(Éčµ±Ź±ŹµŃéĢõ¼žĻĀĘųĢåĦ¶ūĢå»żĪŖV mL/mol)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com