
(12分)(1)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 Ki = 1.75×10-5
碳酸 Ki 1= 4.30×10-7 Ki 2 = 5.61×10-11
亚硫酸 Ki 1= 1.54×10-2 Ki 2 = 1.02×10-7
写出碳酸的第一级电离平衡常数表达式:Ki = _ __
在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性最强的是
③ 若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是 (填序号)
A. c(CH3COO-) B. c(H+) C. w醋酸电离平衡常数 D. 醋酸的电离度
 (2)一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数
(2)一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数
Ksp=cm(An+)×cn(Bm-),称为难溶电解质的离子积。在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。
下列叙述不正确的是  w.w.w.zxxk.c.o.m
w.w.w.zxxk.c.o.m
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KCl溶液,则无白色沉淀产生
C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
(3)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是 (填“A”或“B”)。

设盐酸中加入的Zn质量为m1, 醋酸溶液中加入的Zn质量为m2。则m1 m2(选填“<”、“=”、“>”)
(1)① 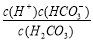 ② H2CO3 ③ A D (2)C
② H2CO3 ③ A D (2)C
(3)B,<
【解析】
试题分析:(1)①写出碳酸第一步电离的电离方程式,根据电离平衡常数的表达式得Ki;②电离平衡常数越大,酸性越强,碳酸的酸性看第一步电离的平衡常数,HSO3-的酸性看亚硫酸的第二步电离的平衡常数Ki2;③加入盐酸,氢离子浓度增大,醋酸的电离平衡向左移动,电离程度减小,醋酸根离子的浓度减小,氢离子的浓度增大,电离平衡常数只与温度有关,故电离平衡常数不变,故选AD;(2)A、难溶的可以转化成更难溶的,故A正确;B、先生成了硫化银沉淀,因氯化银的溶解能力大,故不能转化成氯化银沉淀,故B正确;因三者的Ksp不相同,即溶解能力不相同,故三者的饱和溶液中的银离子的浓度不相同,故C错误;D、溶度积只与温度有关,与在哪种溶液中无关,故在两种溶液中的溶度积相同,故D正确;故选C;(3)开始时两溶液中的氢离子浓度相等,醋酸溶液中还存在醋酸的电离平衡,随着反应的进行,氢离子的消耗,醋酸的电离平衡向右移动,使氢离子的浓度增大,故醋酸溶液中的氢离子浓度减小的慢,故B曲线是醋酸;在pH相等,即开始氢离子浓度相等的条件下,醋酸的物质的量浓度大,故在体积相等的条件下,醋酸消耗的锌多。
考点:电离平衡常数的表达式、电离平衡的影响因素、溶解平衡的影响因素、溶度积的影响因素等知识。


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源:2013-2014江苏省高三模拟考试化学试卷(解析版) 题型:选择题
下列表示对应化学反应或过程的离子方程式正确的是
A.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
B.碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
C.用石墨作电极电解AlCl3溶液:2Cl-+2H2O  Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.亚硫酸氢钠溶液显酸性:NaHSO3=Na++H++ SO32-
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省徐州市高三第三次模拟考试化学试卷(解析版) 题型:选择题
短周期主族元素A、B、C、D、E的原子序数依次递增,A的单质在常温下呈气态,D元素的单质既能与盐酸反应也能与NaOH溶液反应,B、C、E原子的最外层电子数之和为13,E原子的最外层电子数是B原子内层电子数的3倍或是C原子最外层电子数的3倍。下列说法正确的是( )
A. 原子半径的大小顺序:r(B)>r(C)>r(A)
B. 元素E的氧化物的水化物一定是强酸
C. D单质在一定条件下可以与氧化铁发生置换反应
D. 工业上常用电解元素C、D的氯化物来制取它们的单质
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高一下学期5月段考化学必修试卷(解析版) 题型:选择题
下列反应属于加成反应的是
A.2CH3CH2OH + 2Na →2CH3CH2ONa + H2↑
B.
C.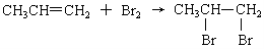
D.
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省吴江市高二下学期期中考试化学试卷(解析版) 题型:选择题
由可逆反应绘出图像如图,纵坐标为生成物在平衡混合物中的百分含量,下列对该反应的判断正确的是 ( )

A.反应物中一定有气体 B.生成物中一定有气体
C.正反应一定是放热反应 D.正反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省吴江市高二下学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式中,正确的是
A.用惰性电极电解MgCl2溶液:2Cl—+H2O通电 2OH—+Cl2↑+H2↑
B.碳酸钠溶液显碱性:CO32—+H2O HCO3—+OH—
HCO3—+OH—
C.氯气通入冷水中:Cl2 +H2O  Cl- +ClO- +2H+
Cl- +ClO- +2H+
D.碳酸镁悬浊液中加醋酸:CO32-+2CH3COOH = 2CH3COO-+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省吴江市高一下学期期中考试化学试卷(解析版) 题型:选择题
能正确表示下列化学反应的离子方程式的是
A.小块金属钠投入水中:Na+2H2O=Na++2OH-+H2↑
B.铝片投入氢氧化钠溶液中: 2Al+2OH-+2H2O= 2AlO2-+3H2↑
C.H2SO4溶液中滴入Ba(OH)2溶液:Ba2++OH-+H++SO42-= BaSO4↓+H2O
D.铁钉投入稀盐酸中:Fe +2H+= Fe2++H2↑
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省2013-2014学年高三模拟考试化学试卷(解析版) 题型:选择题
某恒温密闭容器中,可逆反应A(s)  B+C(g) ΔH= +Q kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
B+C(g) ΔH= +Q kJ·mol-1(Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1
C. 若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q kJ
D. 保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com