
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol?L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、c1=c2 |
| B、a+b=92.4 |
| C、2p2=p3 |
| D、α2>α3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
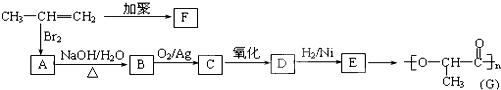
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中Ca2+离子数目减少 |
| B、溶液中c(Ca2+)增大 |
| C、溶液的pH增大 |
| D、溶液中溶质的质量分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是干冰的晶胞结构示意图.请完成下列问题:
如图是干冰的晶胞结构示意图.请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
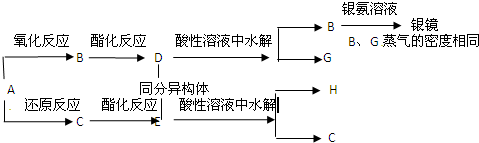
查看答案和解析>>
科目:高中化学 来源: 题型:
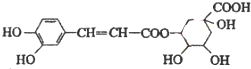
| A、分子式为C16H15O9 |
| B、不能与NaHCO3溶液反应 |
| C、能发生取代反应和消去反应 |
| D、1 mol绿原酸最多与可8mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com