
【题目】下列物质中既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3②(NH4)2S③Al(OH)3④NH4Cl⑤H2N-CH2-COOH ⑥CH3COOH
A. ①②③ B. ①②④⑤ C. ⑤⑥ D. ①②③⑤
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵(NH4)aFeb(SO4)cdH2O又称莫尔盐,是浅绿色晶体。用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如下:

已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,反应Ⅰ如下:FeS2 + 14Fe3+ + 8H2O =15Fe2+ + 2SO42— + 16H+
(1)写出“还原”时Fe3+与FeS2发生还原反应Ⅱ的离子方程式:______。实验室检验“还原”已完全的方法是_______________。
(2) “还原”前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
离子 | 离子浓度(mol·L-1) | |
还原前 | 还原后 | |
SO42- | 3.20 | 3.40 |
Fe2+ | 0.05 | 2.15 |
请计算反应Ⅰ、Ⅱ中被还原的Fe3+的物质的量之比______。
(3)称取11.76g新制莫尔盐,溶于水配成250mL溶液。取25.00 mL该溶液加入足量的BaCl2溶液,得到白色沉淀1.398 g;另取25.00 mL该溶液用0.0200 mol/L KMnO4酸性溶液滴定,当MnO4-恰好完全被还原为Mn2+时,消耗溶液的体积为30.00mL。试确定莫尔盐的化学式_________________(请写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列几种措施:①对燃烧煤时产生的尾气进行除硫处理 ②少用原煤做燃料 ③燃烧煤时鼓入足量空气 ④开发清洁能源。其中能减少酸雨产生的措施是( )
A.①②③ B.②③④ C.①②④ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol的镁、铝混合物溶于100 mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。

当V1=160mL时,则金属粉末中n(Mg)=________ mol,V2=_____________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) _____________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组用浓度为0.20mol·L-1的盐酸标准液滴定含有一定量杂质的烧碱样品(杂质与酸不反应)溶于水形成的溶液。

(1)准确量取一定体积的待测液需要使用的仪器是______________。
(2)若滴定开始和结束时,滴定管中的液面如图所示,则消耗盐酸标准液的体积为________mL。
(3)滴定时,若以酚酞为指示剂,滴定达到终点的标志是______________________________。
(4)将准确称取的5.0g烧碱样品配制成250mL待测液,并用盐酸标准液滴定。滴定前读数及滴定后读数如下表所示。
滴定次数 | 待测液体积(mL) | 0.20mol·L-1的盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 10.00 | 0.70 | 20. 60 |
第一次 | 10.00 | 4.00 | 24.10 |
第三次 | 10.00 | 1.10 | 21.10 |
由实验数据可知,烧碱的纯度为__________。
(5)下列操作会导致测得的待测液的浓度偏大的是________(填字母)。
a.部分标准液滴出锥形瓶外 b.用待测溶液润洗锥形瓶
C.锥形瓶洗净后还留有蒸馏水 d.放出碱液的滴定管开始有气泡,放出液体后气泡消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关蛋白质的叙述正确的是( )
A. 蛋白质溶液中,加入浓的硫酸铵溶液有沉淀析出,加水后沉淀不溶解
B. 蛋白质属于天然高分子化合物
C. 蛋白质的分子能透过半透膜
D. 蛋白质与浓盐酸作用时呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应2NaClO2+Cl2═2ClO2+2NaCl.下图是实验室用于制备和收集一定量较纯净的ClO2的装置(某些夹持装置和垫持用品省略)其中E中盛有CCl4液体(用于除去ClO2中的未反应的Cl2).
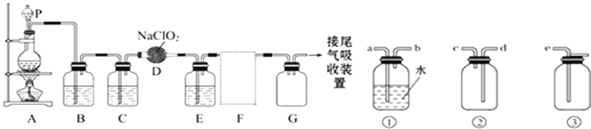
(1)仪器P的名称是________________.
(2)写出装置A中烧瓶内发生反应的离子方程式:__________________________________.
(3)B装置中所盛试剂是________________.
(4)F处应选用的收集装置是__________(填序号或或),其中与E装置导管相连的导管口是_________(填接口字母).
(5)G装置的作用是__________________________________.
(6)若用100mL2molL1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量是______(填序号).
A.>0.1molB.0.1molC.<0.1molD.无法判断。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质E可做香料,其结构简式为![]() ,工业合成路线如下:
,工业合成路线如下:
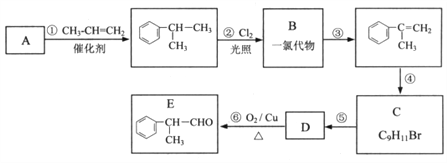
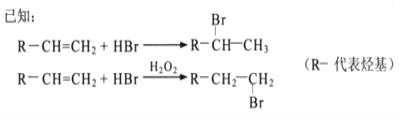
回答下列问题:
(1)A为芳香烃,相对分子质量为78。下列关于A的说法中,正确的是__________(填序号);
a. 所有原子均在同一平面上 b. 密度比水大 c. 一氯代物只有一种
(2)B的结构简式可能是____________________ 、_________________;
(3)D的结构简式为:________________________;
(4)步骤④的化学方程式是____________________________________________;
(5)步骤⑥的化学方程式是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Na+浓度为0.5molL﹣1的某澄清溶液中,还可能含有下表中的若干种离子:
阳离子 | K+、Ag+、Mg2+ |
阴离子 | NO3﹣、CO32﹣、SiO32﹣、SO42﹣ |
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
Ⅲ | 在Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
试回答下列问题:
(1)实验Ⅰ能确定一定不存在的离子是 .
(2)实验Ⅰ中生成沉淀的离子方程式为 .
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
阴离子 | NO3﹣ | CO32﹣ | SiO32﹣ | SO42﹣ |
c/molL﹣1 |
(4)判断原溶液中K+是否存在,若存在,求其最小物质的量浓度,若不存在,请说明理由: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com