
| A. | 体心立方是金属最密堆积形式 | |
| B. | NaCl晶体的配位数为4 | |
| C. | 24g金刚石中含有C-C键的个数为4NA | |
| D. | 中和热测定时,用铜棒代替环形玻璃棒会导致△H偏低 |
分析 A、六方最密堆积和面心立方最密堆积空间利用率最高;
B、NaCl晶体中Na+配位数为6;
C、金刚石中每个C都与另外4个C相连,则平均每个C原子成键数目为4×$\frac{1}{2}$=2个;
D、根据铜棒导热,使反应中放出的热量散失.
解答 解:A、六方最密堆积和面心立方最密堆积是空间利用率最高的结构,是金属最密堆积的形式,故A错误;
B、NaCl晶体中Na+配位数为6,而不是4,故B错误;
C、金刚石中每个C都与令外4个C相连,则平均每个C原子成键数目为4×$\frac{1}{2}$=2个,24g金刚石中含C原子的物质的量为2mol,则含有C-C键的个数为4NA,故C正确;
D、根据铜棒导热,使反应中放出的热量散失,会导致△H偏低,故D正确;
故选CD.
点评 本题考查了晶体结构,明确晶胞结构是解决本题的关键,难点是配位数的计算,难度中等.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 粒子半径:Al3+<Mg2+<F- | B. | 热稳定性:H2Te>H2Se>H2S>H2O | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 金属性:Li<Na<K |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
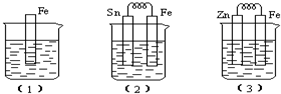
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO32-+H2O?HSO3-+OH- | B. | CO32-+2H2O?H2CO3+2 OH- | ||
| C. | HS-+H2O?H3O++S2- | D. | Al3++3H2O=Al(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同周期元素原子的第一电离能从左往右越来越大 | |
| B. | 同族元素原子从上到下第一电离能越来越大 | |
| C. | 同周期元素原子的电负性从左往右越来越大 | |
| D. | 同族元素原子从上到下电负性越来越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH═CH-CH3 二丁烯 | B. | 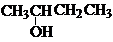 2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3OOCC2H5 乙酸乙酯 | D. | CH3CH(CH3)CH2COOH 3-甲基丁酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com