
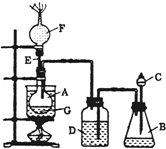
 为了证明乙醇分子中含有氧原子,某小组设计了如图装置进行 实验研究.图中烧杯A用作水浴器,锥形瓶B中盛有试剂X,分液漏斗C和广口瓶D中均盛有浓硫酸,E是一根直导管,干燥管F中填满新制的碱石灰,烧瓶G中装有无水乙醇和一些新制白色无水盐粉末Y.打开C处活塞,将浓硫酸慢慢滴入B中与试剂X作用,之后发现D瓶的导管口产生大量气泡,水浴加热G瓶,不久又观察到G瓶中试剂Y变色,F端排出的气体经净化后还能点燃.请回答下列问题:
为了证明乙醇分子中含有氧原子,某小组设计了如图装置进行 实验研究.图中烧杯A用作水浴器,锥形瓶B中盛有试剂X,分液漏斗C和广口瓶D中均盛有浓硫酸,E是一根直导管,干燥管F中填满新制的碱石灰,烧瓶G中装有无水乙醇和一些新制白色无水盐粉末Y.打开C处活塞,将浓硫酸慢慢滴入B中与试剂X作用,之后发现D瓶的导管口产生大量气泡,水浴加热G瓶,不久又观察到G瓶中试剂Y变色,F端排出的气体经净化后还能点燃.请回答下列问题:分析 (1)浓盐酸与浓H2SO4混合产生HCl气体;
(2)浓硫酸具有吸水性,浓盐酸具有挥发性;
(3)D中所装浓硫酸的作用是除去氯化氢中的水蒸气;
(4)醇能和氢卤酸发生取代反应得到卤代烃;
(5)F中填满新制的碱石灰的目的是防止空气中水蒸气进入干扰检验,E导管除了有导气的基本功能外,在本实验中还具有的作用是冷凝回流;
(6)无水硫酸铜遇到水变化为蓝色,乙醇能和氢卤酸发生取代反应得到卤代烃和水,水中的氧原子来自乙醇.
解答 解:因浓盐酸与浓H2SO4混合产生HCl气体,使干燥的HCl气体在装置A中与乙醇发生反应:C2H5OH+HCl→C2H5Cl+H2O,产生的水可使无水CuSO4变蓝,来证明产生的H2O中的氧元素来源于乙醇,而非HCl,达到验证实验的目的.
(1)实验过程中,HCl气体是利用浓盐酸与浓H2SO4混合制得,故答案为:C;
(2)C中浓硫酸的主要作用是吸收浓盐酸中混有的水分,浓H2SO4溶于水放热,有利于HCl气体逸出,B中逸出的气体成分是HCl和水蒸气,
故答案为:溶解放热,促进HCl挥发; HCl和水蒸气;
(3)用浓盐酸与浓H2SO4混合产生的HCl气体中含有一定量的水蒸气,对水的检验形成强烈干扰,因此一定设法将其除去,故答案为:干燥HCl气体;
(4)乙醇能和氢卤酸发生取代反应,方程式为:CH3CH2OH+HCl$\stackrel{△}{→}$CH3CH2Cl+H2O,
故答案为:CH3CH2OH+HCl$\stackrel{△}{→}$CH3CH2Cl+H2O;
(5)F中填满新制的碱石灰的目的是防止空气中水蒸气进入干扰检验,E导管除了有导气的基本功能外,在本实验中还具有的作用是冷凝回流乙醇等挥发性物质,
故答案为:防止空气中的水蒸气倒吸,冷凝回流;
(6)能证明乙醇分子中含有氧原子的理由是:无水CuSO4变蓝证明了反应中一定有水生成,无水盐粉末Y的化学式是CuSO4,水中的氧元素不能来自于HCl,故只能由乙醇提供,
故答案为:CuSO4;试剂Y由白色变蓝色.
点评 本题考查了证明乙醇分子中含有氧原子实验方案的设计,侧重考查乙醇的化学性质,题目难度中等.注意利用取代法结合质量守恒定律确定乙醇所含元素.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素在自然界中都是以化合态存在于海水,矿物中 | |
| B. | 通常情况下,金属具有导电性、导热性、和延展性 | |
| C. | 金属活动性顺序表中排在氢前的金属都能与酸反应置换出酸中的氢 | |
| D. | 合金的硬度,熔点一般比组成金属高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 35:56 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2 | B. | ZnCl2 | C. | BaCl2 | D. | KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新材料包括新型无机非金属材料和功能有机高分子材料 | |
| B. | 制作光导纤维的材料是单晶硅 | |
| C. | 美国国家实验室制备的类似于二氧化硅结构的二氧化碳原子晶体与干冰属于同分异构体 | |
| D. | 有机高分子材料全部是通过加聚反应或缩聚反应合成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
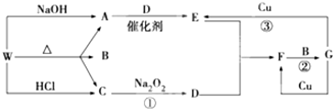
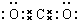 ,F的颜色红棕色.
,F的颜色红棕色.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com