
| Kw |
| Ka |
| 10-14 |
| 10-6 |
| Kw |
| Ka |
| 10-14 |
| 10-6 |


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
| A、该反应的还原剂是CO2 |
| B、该反应的氧化剂是Na2O2,发生氧化反应 |
| C、氧化剂和还原剂的物质的质量比为39:22 |
| D、若有2 mol Na2O2参加反应,则转移电子2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、NiO(OH) |
| B、Ni(OH)2 |
| C、H2 |
| D、H2和NiO(OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
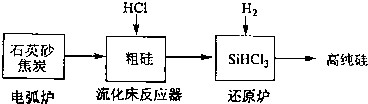
| 发生的主要反应 | |||||
| 电弧炉 | SiO2+2C
| ||||
| 流化床反器 | Si+3HCl
| ||||
| 还原炉 | SiHCl3+H2
|
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,在2L的密闭容器中,发生下述反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol
一定条件下,在2L的密闭容器中,发生下述反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:
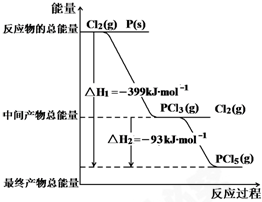 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据).根据图示,回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据).根据图示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
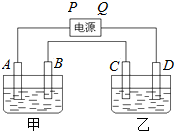 已知A、B、C、D都是铂电极,P、Q是直流电源的两极,通电后发现B极质量增加.
已知A、B、C、D都是铂电极,P、Q是直流电源的两极,通电后发现B极质量增加.查看答案和解析>>
科目:高中化学 来源: 题型:
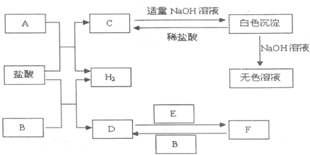 下列物质A~F是我们熟悉的单质或化合物,其中A、E均为C中元素形成的单质,B是常见的金属,且B的合金用量最大;在适当的条件下,它们之间可以发生如图所示的转化.
下列物质A~F是我们熟悉的单质或化合物,其中A、E均为C中元素形成的单质,B是常见的金属,且B的合金用量最大;在适当的条件下,它们之间可以发生如图所示的转化.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、农业废弃物、城市与工业有机废弃物及动物粪便中都蕴藏着丰富的生物质能 |
| B、羊毛、过氧化氢酶、牛胰岛素、血红蛋白、人造奶油充分水解均可得到氨基酸 |
| C、石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向 |
| D、多植树造林,使用“乙醇汽油”,改燃煤为燃气,外出时使用PM2.5口罩等都是治理“雾霾”等灾害性天气的有效措施 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com