
| A. | 乙醇与浓氢溴酸反应:CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O | |
| B. | 溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr | |
| C. | 苯酚钠中通入二氧化碳:2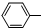 ONa+CO2+H2O→2 ONa+CO2+H2O→2 OH+Na2CO3 OH+Na2CO3 | |
| D. | 淀粉在稀硫酸作用下水解:(C6H10O5)n(淀粉)+nH2O$→_{△}^{稀硫酸}$nC6H12O6 |
分析 A.乙醇与浓氢溴酸,发生取代反应生成溴乙烷和水;
B.溴乙烷与氢氧化钠溶液共热,发生水解反应生成乙醇;
C.碳酸酸性强于酚,酚的酸性强于碳酸氢根离子,苯酚钠中通入二氧化碳反应生成苯酚和碳酸氢钠;
D.淀粉属于多糖,在稀硫酸作用下水解生成葡萄糖.
解答 解:A.乙醇与浓氢溴酸反应,醇羟基被溴原子取代,反应为CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O,故A正确;
B.溴乙烷与氢氧化钠溶液共热的反应为CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr,属于水解反应,故B正确;
C.苯酚钠中通入二氧化碳的反应为C6H5ONa+CO2+H2O→C6H5OH↓+NaHCO3,故C错误;
D.淀粉在稀硫酸作用下水解生成葡萄糖:(C6H10O5)n(淀粉)+nH2O$→_{△}^{稀硫酸}$nC6H12O6,故D正确;
故选C.
点评 本题考查有机物化学反应书写的正误判断,为高频考点,把握常见有机物的性质、有机反应为解答的关键,侧重取代反应及强酸制取弱酸反应的考查,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2晶体中阴离子的个数为2NA | |
| B. | 标准状况下,2.24L苯所含的分子总数为0.1NA | |
| C. | 32gO2和32g O3的所含的氧原子数都是为2NA | |
| D. | 6.4g铜与过量的浓硝酸完全反应转移的电子数是0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4>H2SO4>H3AsO4>H3PO4 | |
| B. | 碱性:Ca(OH)2>Mg(OH)2>Al(OH)3 | |
| C. | 金属单质置换出氢的能力:Cs>Rb>K>Ca | |
| D. | 氧化性:F2>Cl2>S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
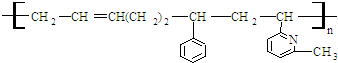
 ②CH2=CH
②CH2=CH ③CH2=CH-CH═CH2④CH3-CH═CHH-CH2
③CH2=CH-CH═CH2④CH3-CH═CHH-CH2
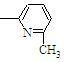 ⑥CH2=CH
⑥CH2=CH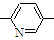 CH3
CH3| A. | ②③⑥ | B. | ②③⑤ | C. | ①②⑥ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
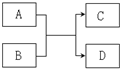 用化学用语回答下面的问题
用化学用语回答下面的问题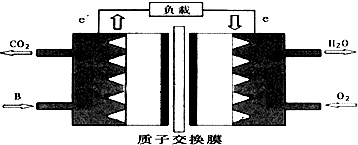
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
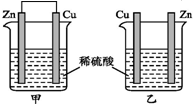
| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中溶液的酸性均减弱 | D. | 产生气泡的速率甲比乙慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
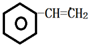 ,C的结构简式:
,C的结构简式: .
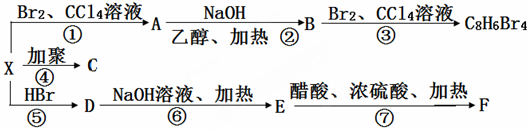
.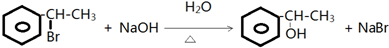 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com