
【题目】乙烯产量是衡量一个国家石油化工水平的主要标志。下图是由乙烯合成乙酸乙酯可能的合成路线:

请回答下列问题:
(1)反应④的化学方程式为_____________________________ ;
(2)在实验室制备乙酸乙酯时,用到饱和的碳酸钠溶液,其作用是:___________________;
(3)乙醇的结构式为 ,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 _________________________________;
,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 _________________________________;
(4)乙酸乙酯的同分异构体(只含一种官能团)有______________种;
【答案】2CH3CH2OH + O2![]() 2CH3CHO + 2H2O 吸收挥发出来的乙酸和乙醇;降低乙酸乙酯的溶解度 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑ .5
2CH3CHO + 2H2O 吸收挥发出来的乙酸和乙醇;降低乙酸乙酯的溶解度 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑ .5
【解析】
(1) 乙醇含有羟基,可以被催化氧化产生乙醛;
(2)从制取乙酸乙酯的反应物及生成物的的物理性质、化学性质和物质的分离提纯分析;
(3)与Na反应生成氢气的量可说明含1个特殊H原子;
(4)根据乙酸乙酯的分子式及题干要求写出符合要求的同分异构体,据此分析解答。
(1)乙醇分子中含有羟基,在Cu作催化剂时,在加热条件下,发生氧化反应,产生乙醛和水,反应的化学方程式是:2CH3CH2OH + O2![]() 2CH3CHO + 2H2O ;
2CH3CHO + 2H2O ;
(2)乙醇和乙酸在浓硫酸催化下,在加热时发生酯化反应,产生乙酸乙酯和水。乙醇、乙酸沸点低,加热容易挥发,反应产生的乙酸乙酯及未反应的乙醇、乙酸通过导气管进入到盛有饱和碳酸钠溶液的试管中,饱和碳酸钠溶液的作用是吸收乙醇、中和乙酸、降低乙酸乙酯溶解度;
(3)实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
(4) 乙酸乙酯分子式是C4H8O2,它的同分异构体,且只含有一种官能团的物质有酯、羧酸;属于酯类的有HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3CH2COOCH3;羧酸有CH3CH2CH2COOH、 (CH3)2 CHCOOH,因此共有5种同分异构体。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】锂空气电池是一种用锂作负极,以空气中的氧气作为正极反应物的电池。其工作原理如图,下列说法中错误的是( )

A. 多孔电极可以提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 正极的电极反应:![]()
C. 有机电解液可以是乙醇等无水有机物
D. 充电时专用充电电极可防止空气极腐蚀和劣化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼(Mo)是一种难熔稀有金属,我国的钼储量居世界第二。钼及其合金在冶金,农业、电器、化工、环保等方面有着广泛的应用。
(1)已知:①2Mo(s)+3O2(g)=2MoO3(s) ΔH1
②MoS2(s) +2O2(g)=Mo(s)+2SO2(g) ΔH2
③2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g) ΔH3
则ΔH3 =________________(用含ΔH1、ΔH2的代数式表示),在反应③中若有0.2mol MoS2参加反应,则转移电子_______________mol。
(2)密闭容器中用Na2CO3(S)作固硫剂,同时用一定量氢气还原辉钼矿(MoS2)的原理是:MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s) +2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示:
Mo(s) +2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示:

①由图可知,该反应的ΔH_____0(填“>”或“<”);P2__________0.1MPa(填“>”或“<”)。
②如果上述反应在体积不变的密闭容器中达平衡,下列说法错误的是______(选填编号)。
A.v正(H2)=v逆(H2O)
B.再加入MoS2,则H2转化率增大
C.容器内气体的密度不变时,一定达平衡状态
D.容器内压强不变时,一定达平衡状态
③由图可知M点时氢气的平衡转化率为________ (计算结果保留0.1%)。
④平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。求图中M点的平衡常数Kp=________________________(MPa)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)10种元素中,化学性质最不活泼的是__________;
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是__________;
(3)元素⑦的氢化物分子式为__________,该氢化物常温下和元素①的单质反应的离子方程式是__________,该氢化物与元素⑧的单质反应的离子方程式是__________;
(4)①和⑧的最高价氧化物对应的水化物化学式为__________和__________。①和⑨两元素形成化合物的化学式为__________,该化合物灼烧时焰色为__________,该化合物的溶液与元素⑧的单质反应的离子方程式为__________;
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)
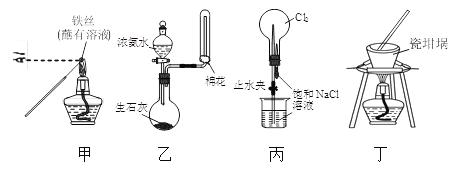
A. 用装置甲检验溶液中是否有K+
B. 用装置乙制取并收集少量NH3
C. 用装置丙进行喷泉实验
D. 用装置丁加热熔融NaOH固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如下,用![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3,下列说法正确的是
分别表示N2、H2、NH3,下列说法正确的是


A. 使用催化剂,合成氨反应放出的热量减少
B. 在该过程中,N2、H2断键形成N原子和H原子
C. 在该过程中,N原子和H原子形成了含有非极性键的NH3
D. 合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其化学方程式是_____________。
(2)验证氯气的氧化性强于碘的实验现象是__________。
(3)B中溶液发生反应的离子方程式是______。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是____________。
(5)过程Ⅲ实验的目的是_________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下____,得电子能力逐渐减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图,图2中,x轴表示实验时流入正极的电子的物质的量, 下列说法中不正确的是
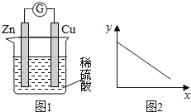
A.y轴可表示锌片的质量
B.y轴可表示溶液中c(H+)
C.若导线上转移2mol电子,则有2molH2生成
D.溶液中的阳离子向正极移动,阴离子向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,V mL不饱和NaNO3溶液a g,蒸发掉b g水或加入b g NaNO3固体(恢复到原温度)均可使溶液达到饱和,则下列各量的计算结果正确的是( )
A. 该温度下NaNO3的溶解度为50 g
B. 原不饱和溶液的密度为![]() g·mL-1
g·mL-1
C. 原不饱和溶液中NaNO3的质量分数为![]() %
%
D. 原不饱和溶液中NaNO3的物质的量浓度为![]() mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com