
���ڿ����о��õ���Ƭ5.0gͶ��ʢ��50mL0.1mol•L-1������Һ���ձ���,����Ƭ�����ᷴӦ����������������v(H2)�뷴Ӧʱ��t�Ĺ�ϵ��������ͼ��ʾ��������������ʾ���������۴������
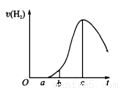
A��O��a�β�������������Ϊ��������������������ϡ����
B��b��c�β����������������ӽϿ����Ҫԭ��֮һ���¶�����
C��t=cʱ�̣���Ӧ����ƽ��
D��t��cʱ���������������ʽ��͵���Ҫԭ������Һ��H��Ũ���½�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������������ѧԺ���и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������£���ȩ�ɷ����֡�������
CH3CHO(l) CH4+CO����֪�÷�Ӧ�Ļ��Ϊ190kJ.mol-1���ں�������I2����Һ�У��÷�Ӧ�Ļ���Ϊ��
CH4+CO����֪�÷�Ӧ�Ļ��Ϊ190kJ.mol-1���ں�������I2����Һ�У��÷�Ӧ�Ļ���Ϊ��
��Ӧ��CH3CHO+ I2 CH3I2+HI+CO ������
CH3I2+HI+CO ������
��Ӧ��CH3I+HI CH4+ I2
CH4+ I2
�����йظ÷�Ӧ����������ȷ���ǣ� ��
A����Ӧ������I2��Ũ���й�
B��HI�ڷ�Ӧ��������������
C����Ӧ�ʱ�ľ���ֵ����190kJ.mol-1
D����ȩ�ķ�Ӧ������Ҫȡ���ڷ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������ˮ�����㣬�ڽ�ˮע�����֮ǰ�������ˮ����������ɹһ��ʱ�䣬��Ŀ����( ��
A������ˮ�еĺ�����
B����ɱ������
C��ʹˮ�еĴ�����ֽ�
D��ʹˮ��Ӳ�ȼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
ͨ����ʳ���Ϳɻ��ij�л�������X������Է�������Ϊ46������̼����������Ϊ52.2%�������������Ϊ13.0%��
��1��X�ķ���ʽ��_______��
��2��X������Ʒ�Ӧ�ų�H2����Ӧ��ѧ����ʽ��_______���л����ýṹ��ʽ�����
��3��X������е�������ͭ�������·�Ӧ����Y��Y�Ľṹ��ʽ��______________��
��4��X��������������Һ��Ӧ������Z���ڼ��Ⱥ�Ũ���������£�X��Z��Ӧ������һ����ɫ����ˮ����ζ��Һ��W��װ����ͼ��ʾ��

������Һ��W�Ļ�ѧ����ʽΪ ��
��Ϊ�˷�ֹa��Һ�屩�У�����ǰӦ��ȡ�Ĵ�ʩ�� ��
��b�Թ��е��ܲ������뵽Һ�����µ������� ��
���Թ�b�м��б���Na2CO3��Һ���������� ��
����184 g X��120 g Z��Ӧ������106 g W����÷�Ӧ�IJ���Ϊ ��
����֪  ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ʵ����ʵ��������Ӧ���۲���ȷ����
��ʵ | ���� | |
A | ������N2������������� | N2�����й��ۼ�ǿ��N2�����ȶ� |
B | �������ڿ�����ȼ��ʱ��Ҫ�ϸ��¶ȣ��������У��������¾Ϳ��Ա����� | ��������������ʱ����߷�Ӧ�¶ȿɼӿ췴Ӧ���� |
C | KI�����HgCl2�����Ϻ�������������һ��Ͷ�뵽ˮ�У��ܿ����ɺ�ɫHgI2 | ��������������ʱ������Ӧ��Ӵ�����ɼӿ췴Ӧ���� |
D | A��B��֧�Թ��зֱ��������5%��H2O2��Һ����B�Թ��м���MnO2 ��ĩ��B�Թ��в������ݿ� | ��������������ʱ���������Լӿ컯ѧ��Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��ӦC2H4(g)+3O2(g)��2CO2(g)��2H2O(g)�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
��v(C2H4)=0.45mol/(L��s) ��v(O2)=0.6mol/(L��s)
��v(CO2)=0.4mol/(L��s) ��v(H2O)=0.45mol/(L��s)
�����йط�Ӧ���ʵıȽ�����ȷ����
A���٣��ڣ��ۣ��� B���ܣ��ۣ��ڣ���
C���ܣ���=�ڣ��� D���٣��ܣ���=��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ʵ����
A��G�����л���������ǵ�ת����ϵ���£�

��ش��������⣺
��1����֪��6.0 g������E��ȫȼ������8.8 g CO2��3.6 g H2O��E������������������ܶ�Ϊ30����E�ķ���ʽΪ ��
��2��AΪһȡ����������B�к���һ��������B����C�Ļ�ѧ����ʽΪ______________��
��3����B����D�ķ�Ӧ������ ����C����D�ķ�Ӧ������ ��
��4��F���������������У���ṹ��ʽΪ________________________��
��5����G��ͬ���칹���У�������һ�����IJ���ֻ��һ�ֵĹ��� �֣����к˴Ź�������������壬�ҷ������Ϊ1��1����___________________����ṹ��ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����л���ѧ��Ӧ������ȡ����Ӧ���� �� ��
A��CH2=CH2��Cl2 �� CH2ClCH2Cl
B��2CH3CH2OH��O2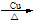 2CH3CHO��2H2O
2CH3CHO��2H2O
C��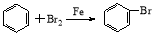 +HBr
+HBr
D��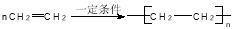
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���½����ܶ��и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ������
I����������Ӱ�����ǵ��������β���ŷ������������������Ҫԭ��֮һ����֪����β���ŷ�ʱ���������·�Ӧ��
��N2��g��+O2��g�� 2NO��g�� ��H1�� a kJ��mol-1
2NO��g�� ��H1�� a kJ��mol-1
��2NO��g��+O2��g�� 2NO2��g�� ��H2�� b kJ��mol-1
2NO2��g�� ��H2�� b kJ��mol-1
��CO��g��+1/2 O2��g�� CO2��g�� ��H3�� c kJ��mol-1
CO2��g�� ��H3�� c kJ��mol-1
��2CO��g��+2NO��g�� N2��g��+2CO2��g�� ��H4
N2��g��+2CO2��g�� ��H4
��ش��������⣺
��1�����ݷ�Ӧ�٢ڢۣ�ȷ����Ӧ���С�H4= kJ��mol-1��
��2�����������˵����Ӧ���Ѵ�ƽ��״̬���� �����ţ���
A����λʱ��������1mol NO2��ͬʱ������lmol NO
B���ں��º��ݵ������У����������ܶȱ��ֲ���
C������������ɫ���ֲ���
D���ں��º�ѹ�������У�NO������������ֲ���
II���״�����Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ��������ʾ��
��ѧ��Ӧ | ƽ�� ���� | �¶�/�� | ||
500 | 700 | 800 | ||
��2H2��g����CO��g�� | K1 | 2.5 | 0.34 | 0.15 |
��H2��g����CO2��g�� | K2 | 1.0 | 1.70 | 2.52 |
��3H2��g����CO2��g�� | K3 | |||
��ش��������⣺
��1����Ӧ���� ������ȡ����ȡ�����Ӧ��
��2���ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3�� ����K1��K2��ʾ����
��3��500 ��ʱ��÷�Ӧ����ijʱ�̣�H2��g����CO2��g����CH3OH��g����H2O��g����Ũ�ȣ�mol��L��1���ֱ�Ϊ0.8��0.1��0.3��0.15�����ʱv�� v�棨���������������������
��4����Ӧ�ٰ�����ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ��
����˵����ȷ����___________________������ţ���

A���¶ȣ�T1��T2��T3
B������Ӧ���ʣ�v��a����v��c����v��b����v��d��
C��ƽ�ⳣ����K��a����K��c����K��b����K��d��
��5������Ч�ļ״�ȼ�ϵ�ز��ò�Ϊ�缫���ϣ����缫�Ϸֱ�ͨ��CH3OH��O2��ij�о�С�齫�����״�ȼ�ϵ�ش�������Ϊ��Դ�����б����Ȼ�����Һ���ʵ�飬��ͼ��ʾ���ش��������⣺
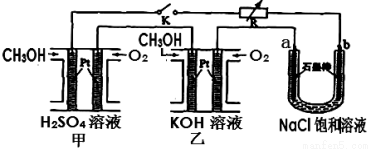
����ȼ�ϵ�صĸ�����ӦʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com