
���� ��1������Ƴ�ԭ��صĻ�ѧ��Ӧ�������Է����еķ��ȵ�������ԭ��Ӧ����������Ƴ�ԭ��أ���������ԭ��Ӧ������Ƴ�ԭ��أ�
��2������Cu+2Ag+�T2Ag+Cu2+��֪FeӦΪ������ʧ���ӱ�������������ΪC��Ag�ȣ�������Ag+�õ�������Ag���������Һ����Ag+�����ݵ����غ�����������ӵ�������
��� �⣺��1����A���÷�Ӧ����������ԭ��Ӧ�����Բ�����Ƴ�ԭ��أ���B���÷�Ӧ���Է����еķ��ȵ�������ԭ��Ӧ����������Ƴ�ԭ��أ���A��NaOH+HCl�TNaCl+H2O�÷�Ӧ�и�Ԫ�صĻ��ϼ۲��䣬���ڸ��ֽⷴӦ�����Բ���������ԭ��Ӧ��������Ƴ�ԭ��أ�
�ʴ�Ϊ����A�����ܣ���B���ܣ���A���÷�Ӧ����������ԭ��Ӧ�����Բ�����Ƴ�ԭ��أ�
��2��Cu+2Ag+=Cu2++2Ag�����ݷ�Ӧǰ��Ľ�������ȷ���缫���ϣ����Ը�ԭ��صĵ缫������ͭ��̼��ͭ��ʧȥ���ӷ���������Ӧ������ͭ���������缫��ӦʽΪ��Cu-2e-=Cu2+��̼������������ԭ��Ӧ��2Ag++2e-=2Ag����������ת�Ƶ���1mol������������1molAg������Ϊ108�ˣ�������������ת�Ƶ���0.1mol����������������10.8g����Ӧ���еĻ�����Ϊ�������ӵĿ����Ի�����������������������Ե������ҺΪ��������Һ��
�ʴ�Ϊ��ͭ��Cu-2e-=Cu2+��������Ӧ��̼��2Ag++2e-=2Ag����ԭ��Ӧ��10.8����������Һ��
���� ���⿼����ԭ��ص���ƺ���ԭ����̽����Ϊ�����ڻ���֪ʶ�Ŀ��飬��Ŀ�ѶȲ��Ƚ����ף�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 1 | B�� | 2 | C�� | 3 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ�صķǽ�����a��b | |
| B�� | a��bֻ���γ����ֻ����ab��ab2 | |
| C�� | c������3��Ԫ�ؾ����γ����ӻ����� | |
| D�� | d��aԪ�����γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| �� | �� | �� | �� | |||||
| �� | �� | �� | �� | �� | �� | �� | ||
| �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
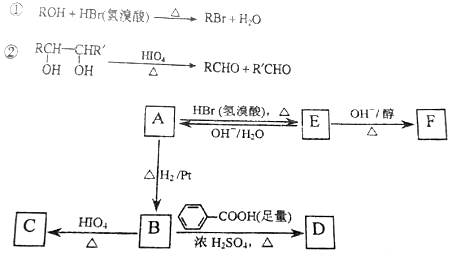
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ������10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������������ʵ�����һ�µ��ǣ� ��
ѡ�� | ʵ����������� | ʵ����� |
A | ��ij��Һ�м��������ữ��BaCl2��Һ,���ɰ�ɫ���� | ����Һ�в�һ������SO42- |
B | ���������������Ũ������,���������� | ���������Ũ�����Ӧ |
C | ����������ˮ�ֱ����FeCl2��Һ��NaI��Һ��,�ٷֱ�μ�CCl4����,�²�ֱ����ɫ���Ϻ�ɫ | ������:Br2>Fe3+>I2 |
D | ��Ũ�Ⱦ�Ϊ0.1 mol��L-1��KCl��KI�����Һ�еμ�1��2��0.01 mol��L-1��AgNO3��Һ,�����ij����ʻ�ɫ | Ksp��AgCl��<Ksp��AgI�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ�����ϵ�һ�ν�ѧ��ϻ�ѧ���������棩 ���ͣ�ѡ����
����������ѧ������д�������
A����Fe��OH��3�����еμ�ϡ���ᣬ�����ɺ��ɫ��������������ܽ�
B����ͭ���м���ϡ���ᣬͭ�۲��ܽ⣬�ټ�������ع��壬ͭ�����ܽ�
C���ȼҵ�ͽ����Ƶ�ұ�����õ���NaCl�������Ϸ����ĵ缫��Ӧ���ǣ�2Cl- - 2e- = Cl2��
D��������[KAl��SO4��2��12H2O]��Һ�е���Ba��OH��2��Һ��SO42��ǡ����ȫ����ʱ�����ӷ���ʽΪ��Ba2++3OH-+Al3++SO42-=BaSO4��+Al��OH��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����A2��g�� + 3B2��g��==2C��g���ķ�Ӧ��˵�����»�ѧ��Ӧ���ʵı�ʾ�У���Ӧ����������
A��v��B2�� =0.9mol/��L•s�� B��v��A2�� =0.4mol/��L•s��
C��v��B2�� =90.0mol/��L•min�� D��v��C�� =36mol/��L•min��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com