


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
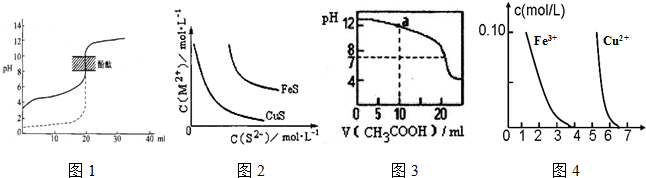
下列装置图或曲线图与对应的叙述相符的是( )

A.图1:负极反应是Fe-2e-=Fe2+
B.图2:酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去
C.图3:可表示乙酸溶液中通入氨气至过量过程中溶液导电性(I )的变化
D.图4:可表示在恒容密闭容器中反应“2SO2(g) +O2(g)2SO3(g) ΔH<0”的平衡常数K正、K逆随温度的变化
查看答案和解析>>
科目:高中化学 来源:2013届福建省三明一中、二中高三上学期期末联考化学试卷(带解析) 题型:单选题
下列装置图或曲线图与对应的叙述相符的是
| A.图1:负极反应是Fe-2e-=Fe2+ |
| B.图2:酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
| C.图3:可表示乙酸溶液中通入氨气至过量过程中溶液导电性(I )的变化 |
D.图4:可表示在恒容密闭容器中反应“2SO2(g) +O2(g) 2SO3(g) ΔH<0”的平衡常数K正、K 2SO3(g) ΔH<0”的平衡常数K正、K |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省、二中高三上学期期末联考化学试卷(解析版) 题型:选择题
下列装置图或曲线图与对应的叙述相符的是

A.图1:负极反应是Fe-2e-=Fe2+
B.图2:酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去
C.图3:可表示乙酸溶液中通入氨气至过量过程中溶液导电性(I )的变化
D.图4:可表示在恒容密闭容器中反应“2SO2(g) +O2(g) 2SO3(g) ΔH<0”的平衡常数K正、K
2SO3(g) ΔH<0”的平衡常数K正、K
随温度的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com