
下列叙述正确的是( )。
A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)·c(OH-)=1×10-14
B.c(H+)=1×10-7 mol·L-1的溶液一定是中性溶液
C.0.2 mol·L-1 CH3COOH溶液中的c(H+)是0.1 mol·L-1 CH3COOH溶液中的c(H+)的2倍
D.任何浓度的溶液都可以用pH来表示其酸性的强弱
解析 KW=c(H+)·c(OH-),且KW只与温度有关,所以,在常温下,纯水、酸性、碱性或中性稀溶液,均有KW=1×10-14;在温度不确定时,中性溶液里的c(H+)不一定等于1×10-7 mol·L-1;0.2 mol·L-1 CH3COOH溶液中的CH3COOH电离程度比0.1 mol·L-1 CH3COOH溶液中的CH3COOH电离程度小,所以,0.2 mol·L-1 CH3COOH溶液中的c(H+)小于0.1 mol·L-1 CH3COOH溶液中的c(H+)的2倍;当c(H+)或c(OH-)大于1 mol·L-1时,用pH表示溶液的酸碱性就不简便了,而是直接用c(H+)或c(OH-)来表示。
答案 A


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
下列事实与胶体性质无关的是 (填字母序号)。
A.土壤中离子的吸附和交换过程,有保肥作用
B.由肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
C.水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
D.明矾可用作净水剂
E.臭氧、Cl2均可用于水的消毒净化
查看答案和解析>>
科目:高中化学 来源: 题型:
向三份0.1 mol·L-1CH3COONa溶液中分别加入少量NH4NO3、Na2SO3、FeCl2固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为 ( )。
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,1体积气态烃和一定量氧气混合并充分燃烧后,再冷却至室温,气体体积比反应前缩小了3体积,则气态烃是( )
A.丙烷 B.乙烯 C.丁烷 D.丁炔
查看答案和解析>>
科目:高中化学 来源: 题型:
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0% .
(1)X的电子式是 ;
(2)X与金属钠反应放出氢气,反应的化学方程式是 (有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是 ;
Y能发生银镜反应,Y与银氨溶液的反应的化学方程式是:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.某盐的水溶液呈酸性,该盐一定是强酸弱碱盐
B.弱电解质溶液稀释后,溶液中各种离子浓度一定都减小
C.水的离子积常数KW随着温度的升高而增大,说明水的电离是吸热反应
D.中和相同体积相同pH的盐酸和醋酸溶液所需NaOH的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语书写正确的是( )
A.氯离子的结构示意图: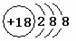 B.作为相对原子质量测定标准的碳核素:
B.作为相对原子质量测定标准的碳核素: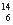 C
C
C.氯化镁的电子式: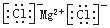
D.用电子式表示氯化氢分子的形成过程:
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是稀硫酸与某金属反应的实验数据:
| 实验序号 | 金属 质量/g | 金属状态 | c(H2SO4) /mol·L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
分析上述数据,回答下列问题:
(1)实验4和5表明, 对反应速率有影响,能表明同一规律的实验还有 (填实验序号);
(2)本实验中影响反应速率的除了浓度还有 ,仅表明该因素对反应速率产生影响的实验有 (填实验序号)。
(3)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
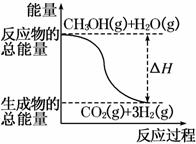 ①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+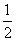 O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
下列说法正确的是 ( )
A.CH3OH的燃烧热为192.9 kJ/mol
B.反应①中的能量变化如下图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+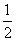 O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol
O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com