
| A、pH=3的盐酸与pH=11的氨水 |
| B、等物质的量浓度的盐酸与氢氧化钾溶液 |
| C、等物质的量浓度的醋酸与氢氧化钠溶液 |
| D、pH=3的醋酸与pH=11的氢氧化钠溶液 |


 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
 根据物质结构与性质的关系,请回答下列问题:
根据物质结构与性质的关系,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、教材所示的铜-锌原电池在工作时,H+、Zn2+向铜片附近迁移 |
| B、电解饱和食盐水时,阳极得到Cl2和NaOH(aq) |
| C、电解铝时,电解槽里的负极材料发生氧化反应 |
| D、原电池与电解池连接后,电子从原电池负极流向电解池阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、压强降低,反应减慢 |
| B、温度降低,反应加快 |
| C、使CO2浓度增加,反应加快 |
| D、使O2浓度增加,反应加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从食盐溶液中获得食盐晶体采用蒸发的方法 |
| B、除去酒精中含有的少量水采用萃取的方法 |
| C、将碘晶体中含有的少量沙子除去采用蒸馏的方法 |
| D、从碘水中获得碘的晶体采用过滤的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向AlCl3溶液中加入过量的氨水,过滤,洗涤,干燥,加热灼烧 | 制取Al2O3 |
| B | 将浓硫酸与碳混合加热,生成的气体通入足量的澄清石灰水 | 检验气体产物中的CO2 |
| C | 将SO2通入品红溶液中,品红溶液褪色,加热褪色后的品红溶液,溶液恢复红色 | 验证亚硫酸的不稳定性 |
| D | 向某溶液中加入NaOH溶液后再加热,若产生的气体能使湿润的红色石蕊试纸变蓝 | 验证该溶液中肯定有NH4+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COONa+CO2+H2O→CH3COOH+NaHCO3 | ||||
B、CH3COOH+CH318OH
| ||||
C、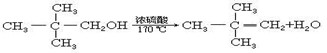 | ||||
D、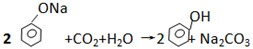 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、H+、SO42- |
| B、Ba2+、NO3-、CO32- |
| C、Al3+、H+、CO32- |
| D、OH-、Fe2+、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com