
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是 ( )
A.A1Cl3 B.Na2O C.NaAl(OH)4 D.SiO2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届山东省高三上学期10月质检化学试卷(解析版) 题型:选择题
从下列事实所列出的相应结论正确的是( )
实 验 事 实 | 结 论 | |
① | SO2使酸性高锰酸钾溶液退色 | 可证明SO2有漂白性 |
② | 用磨口玻璃瓶保存NaOH溶液,用热的纯碱溶液清洗容器里附 | 都发生了氧化还原反应 |
③ | 取少量Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀滴加稀盐酸,沉淀不溶解, | 证明Na2SO3已氧化变质 |
④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
⑤ | 某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
A.①② B.③④ ⑤ C. ②④ D.④ ⑤
查看答案和解析>>
科目:高中化学 来源:2017届山东省临沂市高三上学期期中化学试卷(解析版) 题型:选择题
单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备。
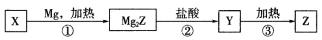
其中X为Z的氧化物;Y为氢化物,分子结构与甲烷相似。下列说法错误的是
A.X可以和氢氟酸反应
B.甲烷的稳定性比Y强
C.Z是将太阳能转换为电能的常用材料
D.上述①②③变化过程中,依次发生置换反应、复分解反应和分解反应
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期10月月考化学试卷(解析版) 题型:实验题
二氧化氯ClO2是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比,ClO2不但具有更显著地杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O
用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是_________________。
(2)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示.(其中 表示氯原子,
表示氯原子, 表示钠原子,
表示钠原子,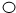 表示氧原子)请写出反应的化学方程式_____________
表示氧原子)请写出反应的化学方程式_____________
(3)消毒水时,ClO2还可将Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,请写出二氧化氯与Mn2+反应的离子方程式____________________。
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样用氢氧化钠溶液调至中性,然后加入一定量的碘化钾,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2=S4O62-+2I-)
Ⅲ.重复上述操作2~3次。
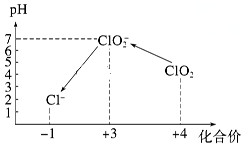
操作时,不同pH环境中粒子种类如下图所示:请回答:
①操作Ⅰ中反应的离子方程式是______________________。
②若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是________mg·L-1。
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期10月月考化学试卷(解析版) 题型:选择题
从下列事实所列出的相应结论正确的是( )
实 验 事 实 | 结 论 | |
① | SO2使酸性高锰酸钾溶液退色 | 可证明SO2有漂白性 |
② | 浓盐酸可除去烧瓶内残留的MnO2,稀硝酸可除去试管内壁的银镜,用磨口玻璃瓶保存NaOH溶液 | 都发生了氧化还原反应 |
③ | 取少量Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀滴加稀盐酸,沉淀不溶解, | 证明Na2SO3已氧化变质 |
④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
⑤ | 某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
A.②⑤ B.①② C.④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省宁德市高二上期中化学试卷(解析版) 题型:实验题
全世界每年被腐蚀损耗的钢铁材料约占全年钢铁产量的十分之一。研究钢铁的腐蚀及防护有重要意义。回答下列问题:
(1)钢铁发生腐蚀的主要类型是电化学腐蚀,在电化学腐蚀中,负极反应是_____________,正极反应是_____________。
(2)某实验小组设计下列实验探究铁生锈的条件:
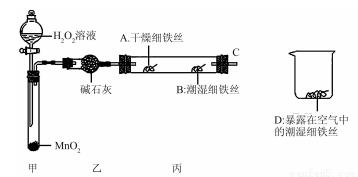
反应4 min后观察,发现A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮。该实验说明铁生锈主要与_________和___________有关;B、D处实验现象对比说明:决定铁生锈的一个重要因素是___________。
(3)金属及塑料制品表面镀铬不仅美观还可提高金属制品抗腐蚀性能。常见镀铬液由重铬酸(H2Cr2O7)和催化剂硫酸组成。
①重铬酸中,Cr元素的化合价为________。
②镀铬时由CrO42-放电产生铬镀层。阴极的电极反应式为_______。
(4)电镀废水中Cr2O72-具有高毒性,必须经处理后才能排放。电解法处理含铬的强酸性废水的原理如右图所示。
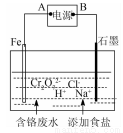
电解产生的Fe2+将Cr2O72-还原为Cr3+,再随着溶液pH的升高,便有Fe(OH)3和Cr(OH)3沉淀生成。
①图中A为电源__________极;电解时阴极产生的气体为____________(写化学式)。
②写出Fe2+与Cr2O72-反应的离子方程式:_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省宁德市高二上期中化学试卷(解析版) 题型:选择题
氯碱工业是以电解饱和食盐水为基础的工业。饱和食盐水是以含Ca2+、Mg2+、SO42-、Fe3+等杂质离子的粗盐水精制,需要使用的药品包括:①稀盐酸 ②烧碱溶液 ③碳酸钠溶液 ④氯化钡溶液。下列有关说法不正确的是( )
A.加入烧碱溶液主要是除去Mg2+、Fe3+
B.药品加入的先后顺序可以是②③④①
C.加入稀盐酸主要是除去所加过量物质中的OH-、CO32-
D.加入碳酸钠溶液主要是除去Ca2+及所加过量物质中的Ba2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:填空题
如图所示,通电5 min时:第③极增重2.16 g,并且观察到A池中只有一个电极在产生气体,通电5min后 ,A池两极均有气体产生。设A池中原混合液的体积为200 mL,求
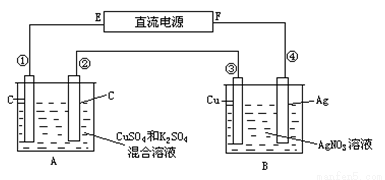
(1)直流电源E是________极;
(2)通电前A池中原混合溶液Cu2+的浓度____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:选择题
在一密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是 ( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是 ( )
A.SO2为0.4mol/L、O2为0.2mol/L B.SO2为0.25mol/L
C.SO2、SO3均为0.15mol/L D.SO3为0.4mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com