
【题目】下列叙述正确的是( )
A.直径介于1~100 nm之间的微粒称为胶体
B.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
C.阳离子只能得到电子被还原,阴离子只能失去电子被氧化
D.含有最高价态元素的化合物不一定具有很强的氧化性
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案科目:高中化学 来源: 题型:
【题目】海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是__________(填物理变化、化学变化);
(2)实验室用MnO2和浓盐酸为原料制备氯气,该反应的化学方程式为________________________________,其中氧化剂是_______还原剂是________。尾气处理的离子方程式为______________________________。
(3)工业上制备漂白粉的化学方程式___________________________________。
(4)将实验室制的氯气配成新制的氯水含有多种微粒,试用方程式或化学式回答下列问题:
将氯水滴加紫色石蕊溶液中,先变红后褪色______________________________(化学方程式)其中,变红后褪色是因为有_________(化学式)生成具有漂白性;
将氯水滴入硝酸银溶液中,有白色沉淀生成__________________________。(离子方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。
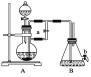
填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是________,A中反应的离子方程式是___________________________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(3)简述生成Fe(OH)2的操作过程:________________________。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为__________________。
(5)下图中________能较长时间看到Fe(OH)2白色沉淀。
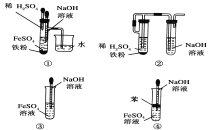
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.阅读、分析下列两个材料:
材料一
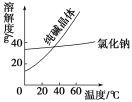
材料二
物质 | 熔点/℃ | 沸点/℃ | 密度/ g/cm3 | 溶解性 |
乙二醇(C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
回答下列问题(填字母序号):
(1)从含少量NaCl的Na2CO3中提纯Na2CO3的操作为溶解、_________、________、过滤、洗涤、干燥
(2)将乙二醇和丙三醇相互分离的最佳方法是_________。
A.蒸馏法 B.萃取法 C.结晶法 D.分液法
II.青蒿素是最好的抵抗疟疾的药物,可从黄花蒿茎叶中提取,它是无色针状晶体,可溶于乙醇、乙醚等有机溶剂,难溶于水。常见的提取方法如下
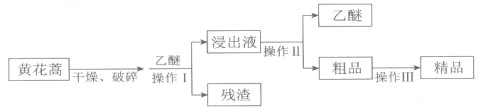
操作I、II中,不会用到的装置是________(填序号)。
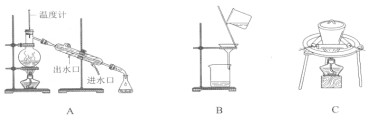
Ⅲ.实验室用98%、密度为1.84g/cm3的浓硫酸配制0.2mol/L的H2SO4溶液470mL.
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、___________、__________。
(2)其操作步骤可分解为以下几步:
A.用量筒量取______mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌。
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
①完成上述步骤中的空白处。
②补充完成正确的操作顺序(用字母填写):____________
( D )→( A )→ → → → →( F )。
(3)下列操作会使所配稀硫酸浓度偏高的是______________。
A、取用浓硫酸时仰视刻度线
B、容量瓶用蒸馏水洗涤后用1.2mol/L的硫酸润洗
C、转移溶液时,不慎有少量溶液洒出
D、定容时仰视容量瓶刻度线
E、将稀释后的稀硫酸立即转入容量瓶且进行后面的实验操作
F、定容后,把容量瓶倒置摇匀,正放后发现液面低于刻度线,又补充几滴 蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,一密闭容器被无摩擦、可滑动的两隔板A、B分成甲、乙两室。标准状况下,在乙室充入8.4g N2,甲室充入8.8g H2和O2的混合气体。
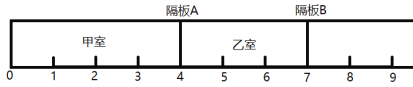
(1)甲室中H2与O2的质量比为_____________,甲室中原子个数约为 ____________个。
(2)维持温度不变,将隔板A固定在“3”处,将隔板B固定在“5”处,此时甲、乙两室中气体的压强比P(甲):P(乙)=______________。
(3)用电火花处理甲室中的气体使其充分反应,反应后恢复至标准状况。甲室与乙室此时的体积比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.01mol·L-1 的醋酸溶液中逐渐加入冰醋酸至1mol·L-1,随着浓度的增加,在一定时间内始终保持减小趋势的是
A. c(H+) B. c(CH3COO-)
C. c(H+)/c(CH3COOH)的比值 D. c(CH3COOH)/c(H+)的比值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,pH=2的两种一元酸HX、HY各取5 mL,分别加水稀释,溶液pH变化与所加水的体积关系如图所示(忽略混合溶液体积的变化),下列说法错误的是
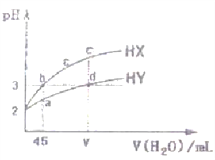
A. 分别取等体积a、b两点溶液,完全中和需同浓度NaOH溶液的体积V(HX)=V(HY)
B. b、d两点溶液中由水电离产生的H+浓度![]()
C. 相同条件下,a、b、c、d、e五点溶液的导电性大小顺序为:a>b=d>c>e
D. 加入NaOH溶液,可以使d点c(Y-)增大、c(H+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的叙述正确的是( )
A.离子化合物中只含离子键
B.共价化合物一定不含离子键
C.离子化合物一定不含共价键
D.共价化合物可能含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的体积主要由以下什么因素决定:( ) ①气体的分子多少 ②气体分子的大小
③气体分子间的平均距离 ④气体分子的相对分子质量.
A.①②
B.①③
C.②③
D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com