
城市大气中铅污染的主要来源是 ( )。
A.铅笔的随意丢弃
B.使用含铅 汽油的汽车尾气
汽油的汽车尾气
C.蓄电池的使用
D.化妆品的大量使用
科目:高中化学 来源: 题型:
用石墨作电极电解下列溶液①稀H2SO4②K2SO4溶液 ③CuCl2溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1的是(填序号)____________
______,其阳极的电极反应式都是____________________________________________,
阴极的电极反应式都是_______________________________________________,
总反应的化学方程式都是_____________________________________________。
(2)阴极、阳极都有气体产生,其中溶液pH变小的是____,pH变大的是______。(填序号)
(3)一个电极析出金属,一个电极逸出气体,且溶液pH明显减小的是____________(填序号),其总反应的化学方程式是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于结构满足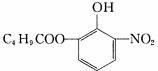 的有机物,下列瞄述中正确的是
的有机物,下列瞄述中正确的是
A、分子中有2种含氧官能团 B、能发生取代、加成、消去、氧化反应
C、1mol该有机物最多消耗3mol NaOH D、苯环上的一溴代物最多有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
汽油是多种烃类的混合物,汽车的发动机中,汽油汽化后与进入汽缸的空气按一定比例混合,在引擎的电火花点燃下燃烧,产生大量热能,但进入汽缸的空气过少或过多都将在汽车尾气中产生有害的大气污染物。目前正在研究和开发一种催化式排气净化器,以Pt—Rh及CuO—Cr2O3作主体催化剂,它可将80%以上的有害尾气转化成无毒气体,但汽油中为增强其抗震性的添加剂(C2H5)4Pb会使这种转化严重降低。下列有关说法中正确的是
( )。
A.汽油的来源是石油的常压、减压分馏
B.机动车必须使用无铅汽油是因为它可使催化剂中毒,制约了催化剂的研
究和开发
C.NO等氮的氧化物对空气的污染是十分严重的,它们不仅使人和动物中毒,
产生疾病,更是破坏大气臭氧层的主要因素
D.如改用柴油作为汽车的燃料,则 可以相对减小汽车尾气对大气的污染
可以相对减小汽车尾气对大气的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气(含有烃类、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂钯合金作催化剂)。它的特点是使CO和NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)下列说法错误的是 。
A.CO和NOx反应的化学方程式为2xCO+2NOx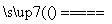 2xCO2+N2
2xCO2+N2
B.上述方法的缺点是由于CO2增多,会大大提高空气的酸度
C.多植树造林,增大绿化面积,可有效控制城市空气各种污染源
D.汽车改用天然气为燃料或开发氢能源,都会减少对空气的污染
(2)写出CO与NO反应的化学方程式_____________________。
(3)“催化转换器”的缺点是在一定程度上提高了空气的酸度,其原因是___________________________________________。
(4)控制城市空气污染源的方法可以有 (填序号)。
A.开发氢能源 B.使用电动车
C.植树造林 D.戴上呼吸面具
( 5)汽车尾气可引起光化学烟雾,主要是 气体。形成酸雨主要是 气体,在尾气转化中,主要还会产生 气体,造成温室效应。
5)汽车尾气可引起光化学烟雾,主要是 气体。形成酸雨主要是 气体,在尾气转化中,主要还会产生 气体,造成温室效应。
查看答案和解析>>
科目:高中化学 来源: 题型:
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10,下列说法中不正确的是( )
A.在t℃时,AgBr的Ksp为4.9×10-13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
 D.在t℃时,AgCl(s)+Br-(aq)
D.在t℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)平衡常数K≈816
AgBr(s)+Cl-(aq)平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D均为中学化学中常见的物质,它们之间转化关系如下图(部分产物已略去):
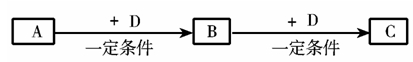
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为 (填元素符号)
(2)若D是金属,C溶液在储存时应加入少量D,其理由是(用必要的文字和离子方程式表示) ;D在潮湿的空气中易发生吸氧腐蚀,写出腐蚀时原电池正极的电极反应式 。
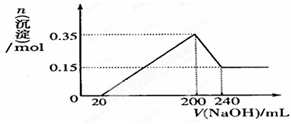
(3)若A、B、C为含同一种金属元素的无机化合物,在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子方程式 。化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E 的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则固体混合物中Mg的质量为 ;NaOH溶液的物质的量浓度为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
某一元弱酸(用HA表示)在水中的电离方程式是:HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向 (填“正”或“逆”)反应方向移动,理由是 。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向 (填“正”或“逆”)反应方向移动,溶液中c(A-)将 (填“增大”“减小”或“不变”),溶液中c(OH-)将 (填“增大”“减小”或“不变”)。
(3)在25℃下,将amol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显 性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com