
【题目】分子式为C9H18O2的有机物A能在酸性条件下进行下列转化,同温同压下,相同质量的B和C的蒸气所占体积相同.则下列说法不正确的是( )(A,B,C,D,E均为有机物) 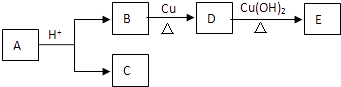
A.符合上述转化关系的有机物A的结构有8种
B.C和E一定为同系物
C.1molB完全转化为D转移2mol电子
D.D到E发生氧化反应
【答案】B
【解析】解:有机物A的分子式应为C9H18O2 , 在酸性条件下甲水解为B和C两种有机物,则有机物A为酯,由于B与C相对分子质量相同,因此酸比醇少一个C原子,说明水解后得到的羧酸含有4个C原子,而得到的醇含有5个C原子,
A、含有4个C原子的羧酸有2种同分异构体:CH3CH2CH2COOH,CH3CH(CH3)COOH;含有5个C原子的醇的有8种同分异构体:CH3CH2CH2CH2CH2OH,CH3CH2CH2CH(OH)CH3 , CH3CH2CH(OH)CH2CH3;CH3CH2CH(CH3)CH2OH,CH3CH2C(OH)(CH3)CH3 , CH3CH(OH)CH(CH3)CH3 , CH2(OH)CH2CH(CH3)CH3;CH3C(CH3)2CH2OH,其中醇能能被氧化成羧酸,说明羟基所连碳上有2个氢原子,共有4种,所以有机物甲的同分异构体数目有2×4=8,故A正确;
B、D与氢氧化铜应在碱性条件下氧化得E应为有机羧酸盐,而C是A在酸性条件下水解得的羧酸,它们不是同系物,故B错误;
C、B中含有羟基,被氧化成醛基,失去2个氢原子,所以1molB完全转化为D转移2mol电子,故C正确;
D、D与氢氧化铜应在碱性条件下氧化得E,即D到E发生氧化反应,故D正确,
故选B;


科目:高中化学 来源: 题型:
【题目】下列实验误差分析正确的是( )
A.用湿润的pH试纸测稀碱液的pH,测定值偏大
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物M是中药狼把草的成分之一,它具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( ) 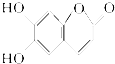
A.M的摩尔质量是180g/mol
B.1 mol M最多能与2 mol Br2发生反应
C.1 mol M与足量NaHCO3反应能生成4 mol CO2
D.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.该电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“﹣”.高铁电池的总反应为: 3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述不正确的是( )
A.放电时正极反应为:FeO ![]() +3e﹣+4H2O=Fe(OH)3↓+5OH﹣
+3e﹣+4H2O=Fe(OH)3↓+5OH﹣
B.充电时阴极反应为:Zn(OH)2+2e﹣=Zn+2OH﹣
C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
D.标有“+”的接线柱充电时作阳极,放电时作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工业生产上容易产生工业“三废”,'变废为宝,探索利用是化学必需要完成的.某工厂的工此废料中含有铜、铝、铁,可利用其制备CuSO45H2O、Fe SO47H2O和AlCl3过程如图: 
(1)将AlCl3溶液蒸干并灼烧,得到的产物是 .
(2)写出A→C的化学方程式: .
(3)检验滤液D中的金属阳离子的方法:
(4)写出E→CuSO4的化学方程式: .
(5)写出废料与烧碱反应的离子方程式: .
(6)取少量滤液D,向其中加入双氧水,现象为: .
(7)用CuSO4溶液作粗铜的精炼液,阴极上发生的电极反应式为: .
(8)钠和铝都是活泼金属,写出工此生产钠的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上需要利用一批回收的含铜废料制造胆矾(CuSO45H2O).该废料中各种成份含量如下:Cu和CuO约占87%,其它为Mg、Al、Fe、Si及其氧化物,还有少量的难溶物质.工艺流程为: 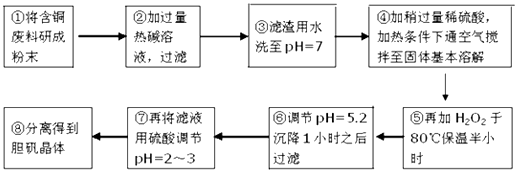
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如表:
沉淀物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 | Fe(OH)2 |
pH | 5.2 | 3.1 | 6.7 | 9.4 | 9.7 |
请回答下列问题:
(1)步骤①中为什么要将含铜废料研磨成粉状? .
(2)步骤②中的离子方程式(写出2个即可):、 .
(3)步骤⑤中H2O2参加反应的离子方程式: .
(4)步骤⑥中调节溶液pH时适宜的物质是(填序号).
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Cu(OH)2 E.MgCO3
(5)步骤⑦中用硫酸调节pH=2~3的原因是 .
(6)步骤⑧的分离方法步骤是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的原子最外层只有一个电子,它与卤素结合时,所形成的化学键( )
A. 一定是离子键
B. 一定是共价键
C. 可能是离子键也可能是共价键
D. 以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由2﹣氯丙烷制取少量的1,2﹣丙二醇 ![]() 时,需要经过下列哪几步反应( )
时,需要经过下列哪几步反应( )
A.消去、加成、取代
B.加成、消去、取代
C.取代、消去、加成
D.消去、加成、消去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com