
科学家一直致力于“人工固氮”的新方法研究。
(1)最新“人工固氮”的研究报道:常温常压.光照条件下,N2在催化剂表面与水发生反应:2N2 (g)+6H2O (l)  4NH3 (g)+3O2 (g)+ Q
4NH3 (g)+3O2 (g)+ Q
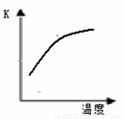
已知该反应的平衡常数K与温度的关系如右图,则此反应的 Q 0 (填“>”“<”或“=”)。
(2)常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, (选填编号)。
A.容器中气体的平均分子量不随时间而变化 B.v(N2)/ v(O2)=2:3
C.容器中气体的密度不随时间而变化 D.通入稀有气体能提高反应的速率
(3)将反应生成的混合气体通入水中即可得氨水。用水稀释0.1mol·L-1氨水,溶液中随着水量的增加而增大的是 (填字母标号)。
A.c(H+)×c(NH3·H2O)/c(OH-) B.c(NH4+)×c(OH-)/c(NH3·H2O)
C.c(H+)·c(OH-) D.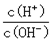
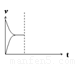
(4)常温下,在恒压密闭容器中上述反应达到平衡后,在其他条件不变时,通入2mol N2,请在右图中画出正(v正).逆(v逆)反应速率随时间t变化的示意图。
(1)< (2)A,B,C
(3)D
(4)
【解析】
试题分析:(1)T升高,K增大,反应是吸热反应,Q<0。
(2)A.该反应不都是气体,m气只有在平衡时不变,可做平衡标志,正确。B.v(N2)和 v(O2)互
为反向速率,v(N2)/ v(O2)=2:3,可做平衡标志,正确;C.m气只有在平衡时不变,可做平衡标志,正确。D.体积不变,稀有气体不参与反应,总体积不变。各反应物质的浓度不变,速率不变,错误。
(3)A.错误;B.加水稀释,c(NH4+)和c(OH-)减小的更多,c(NH4+)×c(OH-)/c(NH3·H2O)减小。C.c(H+)·c(OH-) 只随温度改变,错误;D.c(H+)·c(OH-) 不变,加水稀释,c(OH-)减小,c(H+)增大,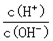 增大,正确。
增大,正确。
(4)改变正反应浓度,逆反应速率是连续的。
考点:本题以化工生产为基础,考查平衡常数与平衡标志,图像等知识。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源:广东省高考真题 题型:填空题


 。设在容积为2.0 L的密 闭容器中充人0. 60 mol N2(g)和l.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。计算
。设在容积为2.0 L的密 闭容器中充人0. 60 mol N2(g)和l.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。计算  的平衡常数。
的平衡常数。 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com