
【题目】已知β锂辉矿(主要成分为LiAlSi2O6 , 还含有FeO、MgO、CaO等杂质),下面是以锂辉矿为原料来制取金属锂的一种工艺流程.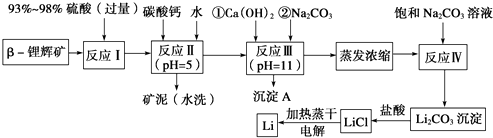
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
请回答下列问题:
(1)为了提高β锂辉矿浸出率可采取措施有 .
(2)反应Ⅰ发生主反应:LiAlSi2O6+H2SO4(浓Li2SO4+++H2O,根据题意配平上述方程式.
(3)反应Ⅱ加入碳酸钙的作用是 .
(4)反应Ⅲ中生成沉淀A成分: . (填化学式)
(5)蒸发浓缩过程中主要发生离子反应方程式: .
(6)洗涤所得Li2CO3沉淀要使用(选填“热水”或“冷水”),你选择的理由是 .
(7)电解熔融氯化锂生产锂时,阳极产生的Cl2中会混有少量O2 , 用电极反应式说明原因 .
【答案】
(1)适当提高溶液的温度或粉碎锂辉矿增大接触面积或多次浸出或延长浸出时间或多次搅拌
(2)2;4;1;Al2(SO4)3;4SiO2↓;4
(3)除去反应Ⅰ中过量的H2SO4;控制pH,使Fe3+、Al3+完全沉淀
(4)Mg(OH)2、CaCO3
(5)2Li++CO32﹣=Li2CO3↓
(6)热水;Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗
(7)加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2 , 2O2﹣﹣4e﹣=O2↑
【解析】解:(1)将硅酸盐改为氧化物形式的方法为:依次将各元素写成氧化物形式,中间用“”连接,同时要注意氧化物先后顺序,为Li2OAl2O34SiO2 , 所以答案是:Li2OAl2O34SiO2;(2)LiAlSi2O6 与H2SO4(浓)反应生成硫酸锂、硫酸铝、二氧化硅和水,结合原子守恒配平得到化学方程式为:2LiAlSi2O6+4H2SO4(浓)=Li2SO4+Al2(SO4)3+4SiO2↓+4H2O,
所以答案是:2,4,1,Al2(SO4)3 , 4SiO2↓,4;(3)β﹣锂辉矿在加入过量浓硫酸后,只有SiO2不溶,同时Fe2+被氧化为Fe3+ , 并生成CaSO4沉淀,所以溶液中含有Fe3+、Al3+、Mg2+、Li+等离子,依据实验目的可知必须除去杂质离子,故在反应Ⅱ中加入碳酸钙的作用为:可除去反应Ⅰ中过量的H2SO4 , 降低溶液中c(H+),根据pH=5,可使Fe3+、Al3+完全沉淀,
所以答案是:除去反应Ⅰ中过量的H2SO4;控制pH,使Fe3+、Al3+完全沉淀;(4)利用题干信息知反应Ⅲ要除去Mg2+ , 但在加入沉淀剂Ca(OH)2时会引入大量Ca2+ , 故还需加入Na2CO3除去Ca2+ , 即沉淀A为Mg(OH)2沉淀与CaCO3沉淀的混合物,反应的离子方程式为:Mg2++2OH﹣═Mg(OH)2↓、Ca2++CO32﹣═CaCO3↓,
所以答案是:Mg(OH)2、CaCO3;(5)蒸发浓缩过程中主要发生锂离子结合碳酸根离子生成碳酸锂,反应的离子方程式为:2Li++CO32﹣=Li2CO3↓,
所以答案是:2Li++CO32﹣=Li2CO3↓;(6)实验室里分离固液混合物的操作是过滤,由题中给出Li2CO3的溶解度与温度的关系,可知洗涤Li2CO3沉淀要使用热水,Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗,
所以答案是:热水;Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗;(7)由有氧气产生可逆推知可能的原因:加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2 ,
所以答案是:加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2 ;


科目:高中化学 来源: 题型:
【题目】根据世界环保联盟的要求,广谱消毒剂ClO2将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,则反应后Na2SO3转化为
A. Na2SO4 B. SO2 C. S D. Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Ⅳ为一种重要化工中间体,其合成方法如下: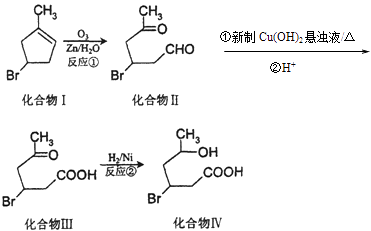
(1)化合物Ⅰ在核磁共振氢谱图吸收峰个数为;反应②的反应类型为 .
(2)化合物Ⅱ与新制Cu(OH)2悬浊液反应,写出该反应的化学方程式 .
(3)化合物I在NaOH醇溶液中加热反应得到化合物X,X的结构简式可能是 . (写出任意一种的结构简式).
(4)化合物III与足量NaOH水溶液加热反应的化学方程式为 .
(5)异黄樟油素 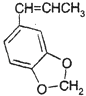 发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为 .
发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为 .
(6)有关上述化合物,说法不正确的是
A.1mol化合物Ⅲ,最多可与2molH2反应
B.化合物Ⅳ在一定条件下能与HBr反应
C.化合物Ⅰ能使酸性高锰酸钾溶液褪色
D.化合物Ⅳ在一定条件下能发生缩聚反应
E.化合物Ⅱ分子式为C6H11O2Br.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种化合物W,X,Y,Z,它们都是由短周期元素A,B,C,D,E中的两种元素组成的.已知: (a)A,B,C,D,E五种元素的原子序数依次增大,且A,D同主族,C,E同主族,B、C同周期.
(b)W由B,C组成,分子中原子个数比为B:C=1:2,固体易升华.
(c)X由A,C组成,分子中原子个数比为A:C=1:1.
(d)Y由C,D形成的离子化合物,且Y中相应元素的微粒之比为:C:D=1:1.
(e)Z是由D,E形成的离子化合物,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1:2.
试回答下列各小题:
(1)各元素符号:ABCDE
(2)W的电子式: .
(3)X的结构式: .
(4)Y的电子式: .
(5)Z的化学式: .
(6)写出Y与水反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示.请依图回答下列问题: 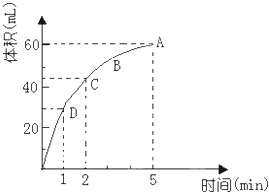
(1)放出一半气体所需要的时间为;
(2)A、B、C、D各点反应速率快慢的顺序是 .
(3)在5min后,收集到的气体体积不再增加,原因是 .
(4)过氧化氢溶液的初始物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出).下列说法错误的是( ) 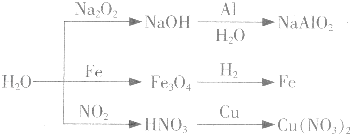
A.如图所示的反应均为氧化还原反应
B.比较镁、铁与水的反应条件,可知铁的金属性比镁弱
C.工业上常用NO2与水的反应原理制取硝酸
D.实验室中可用铜与稀硝酸反应制取NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得101kPa时,1 molH2完全燃烧生成液态水,放出285.8kJ的热量;1 mol CH4完全燃烧生成液态水和CO2 , 放出890.3kJ的热量.下列热化学方程式书写正确的是( )
A.2H2(g)+O2(g)═2H2O(l)△H=﹣285.8 kJmol
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3 kJmol
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3 kJmol
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3 kJmol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )
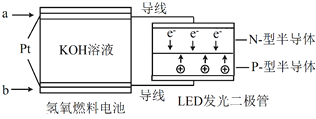
A. 电路中的电子从负极经外电路到正极,再经过KOH溶液回到负极,形成闭合回路
B. a处通入氢气, b处通氧气,该装置将化学能最终转化为电能
C. 电池放电后, OH-的物质的量浓度减小
D. 通入O2的电极发生反应:O2 + 4e- = 2O2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com