
| A. | 棉花 | B. | 光导纤维 | C. | 羊毛 | D. | 蚕丝 |
科目:高中化学 来源: 题型:选择题
| A. | 5、9、6 | B. | 4、9、6 | C. | 3、9、7 | D. | 5、9、10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁与醋酸:Fe2O3+6H+═2Fe3++3H2O | |
| B. | 碳酸钠与盐酸:Na2CO3+2H+═2Na++CO2↑+H2O | |
| C. | 铁片插入到硫酸铜溶液中:2Fe+3Cu2+═2Fe3++3Cu | |
| D. | 向盐酸中加入适量氨水:H++NH3•H2O═NH4++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
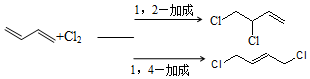
 )的一条路线如图:
)的一条路线如图: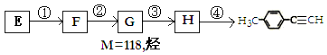
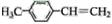 .
. 、
、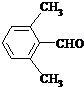 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
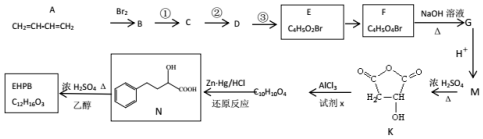
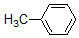 +H3C
+H3C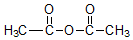 $\stackrel{AlCl_{3}}{→}$
$\stackrel{AlCl_{3}}{→}$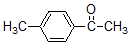 +CH3COOH
+CH3COOH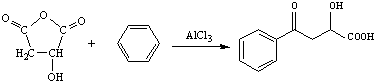 .
.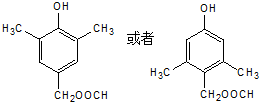 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CO18OC2H5+H2O $?_{△}^{稀硫酸}$ CH3COOH和C2H518OH | |
| B. | 溴乙烷与氢氧化溶液共热:CH3CH2Br+NaOH $→_{△}^{水}$ CH3CH2OH+NaBr | |
| C. | 蔗糖水解: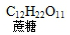 +H2O$\stackrel{催化剂}{→}$ +H2O$\stackrel{催化剂}{→}$ | |
| D. | 苯酚钠中通入二氧化碳: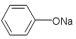 +CO2+H2O→ +CO2+H2O→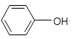 +NaHCO3 +NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
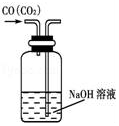 | 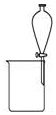 | 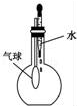 | 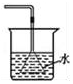 |
| A.除去CO气体中的CO2气体 | B.分离碘酒中的碘和酒精 | C.验证NH3的溶解性 | D.吸收HCl防倒吸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中一定存在SO42-和Cl- | |
| B. | 取③中滤液加入KSCN,溶液显红色,则原溶液一定有Fe3+ | |
| C. | 原溶液中一定不存在Ba2+和HCO3- | |
| D. | 为确定原溶液中是否含有K+,可通过焰色反应直接观察焰色是否为紫色来确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C=O(CO2) | C=O(COS) | C=S | H-S | H-O |
| 键能(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | amol | 0 | 0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com