
【题目】下列大小关系正确的是
A.熔点:己烷>2-甲基丁烷>戊烷>丁烷
B.含氢量:甲烷>乙烷>乙烯>乙炔>苯
C.密度:苯>H2O>CCl4
D.相同物质的量物质完全燃烧耗氧量:己烷>环己烷>苯
【答案】D
【解析】
A.已烷、2-甲基丁烷、戊烷、丁烷,碳原子数的大小顺序为:已烷>戊烷=2-甲基丁烷>丁烷,故熔点的大小顺序为:已烷>戊烷>丁烷,已烷>2-甲基丁烷>丁烷,2-甲基丁烷中含有支链,故沸点的大小顺序为:戊烷>2-甲基丁烷,故故它们的熔点由高到低的顺序为:已烷>戊烷>2-甲基丁烷>丁烷,故A错误;
B.甲烷最简式为CH4,乙烷的最简式为CH3,乙烯的最简式为CH2,乙炔的最简式为CH,苯的最简式为CH,故含氢量为:甲烷>乙烷>乙烯>乙炔=苯,故B错误;
C.苯的密度比水小,四氯化碳的密度比水大,故密度:苯<H2O<CCl4,故C错误;
D.1mol已烷燃烧的耗氧量为:6+![]() =9.5mol,1mol环已烷燃烧的耗氧量为:9mol,1mol苯燃烧的耗氧量为7.5mol,故相同物质的量物质完全燃烧耗量:已烷>环已烷>苯,故D正确,
=9.5mol,1mol环已烷燃烧的耗氧量为:9mol,1mol苯燃烧的耗氧量为7.5mol,故相同物质的量物质完全燃烧耗量:已烷>环已烷>苯,故D正确,
答案选D。


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA为阿伏加德罗常数)( )
A.124gP4含有P—P键的个数为6NA
B.24g石墨中含有六元环个数为3NA
C.46g乙醇中含有极性键的个数为6NA
D.18g冰中含氢键的个数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。

(1)上图所示氮循环中,属于氮的固定的有________(填字母序号)。
a. N2转化为氨态氮 b. 硝化过程 c. 反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一。
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为________。
②检验氨态氮肥中NH4+的实验方案是________。
(3)硝化过程中,含氮物质发生________(填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol氮气时,转移的电子的物质的量为________ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮和硝态氮的原理:________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来食品安全问题成为社会各界日益关注的焦点话题.香港地区食环署食物安全中心曾对十五个桂花鱼样本进行化验,结果发现十一个样本中含有孔雀石绿。孔雀石绿是化工产品,具有较高毒性,高残留,且长期服用后,容易致癌、致畸,对人体有害。其结构简式如图所示。下列关于孔雀石绿的说法正确的是( )

A.孔雀石绿的分子式为C23H25N2
B.1mol孔雀石绿在一定条件下最多可与6molH2发生加成反应
C.孔雀石绿属于芳香烃
D.孔雀石绿苯环上的一氯取代物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请把下列现象中浓硫酸表现出来的性质写填在对应的空白处:
(1)把浓硫酸滴在白纸上,白纸变黑,则浓硫酸表现___(填“脱水性”或“氧化性”);
(2)盛有浓硫酸的烧杯敞口放置一段时间,质量增加,则浓硫酸表现出___(填“吸水性”或“脱水性”);
(3)浓硫酸与碳共热时发生反应2H2SO4(浓)+C![]() CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出___(填“酸性”或“强氧化性”)。
CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出___(填“酸性”或“强氧化性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭的容器中充入2molA和1molB发生反应:2A(g)+B(g)![]() xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mo1充入容器,达到平衡后,C的体积分数仍为w%,则x的值为
xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mo1充入容器,达到平衡后,C的体积分数仍为w%,则x的值为
A. 2 B. 3 C. 2或3 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3、SO2和Cl2是中学化学常见的气体,研究其性质和制备具有重要意义。回答下列问题:
(1)实验室中干燥氨气常用的干燥剂是___(填“碱石灰”或“五氧化二磷”)。
(2)某同学用干燥的圆底烧瓶收集满一瓶干燥氨气,进行喷泉实验并取得成功。说明氨气___(填“极易”或“不易”)溶于水;圆底烧瓶中溶液变红色,说明氨水呈___(填“酸性”或“碱性”)。
(3)某兴趣小组为验证SO2和Cl2的漂白性;设计了如下方案(尾气处理装置未画出)。

①如图甲所示,向品红溶液中通入SO2,同学们发现品红溶液褪色了,停止通气体,加热试管,发现溶液呈___(填“红”或“无”)色;
②如图乙所示,将干燥的Cl2和SO2按体积比1:l混合通入石蕊溶液中,发现石蕊溶液变红,不褪色,用化学方程式解释之:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上已经实现CO2与H2反应合成甲醇。在一恒温、恒容密闭容器中充入2mol CO2和6 mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
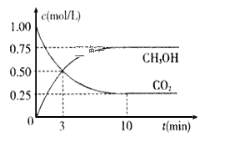
(1)写出该反应的平衡常数表达式_____________________。
(2)达到平衡状态的时刻是__________min(填“3”或“10”)。
(3)在前10min内,用CO2浓度的变化表示的反应速率![]() (CO2)=_________mol/(L·min)。
(CO2)=_________mol/(L·min)。
(4)10min时体系的压强与开始时压强之比为____________。
(5)该温度下,反应的化学平衡常数数值是____________。
(6)已知:①CO(g)+2H2(g)![]() CH3OH(g) ΔH= -90.1kJ·mol-1 ②CO(g)+H2O(g)
CH3OH(g) ΔH= -90.1kJ·mol-1 ②CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-41.1kJ·mol-1,则CO2与H2反应合成CH3OH(g)的热化学方程式为_______________,反应在10 min内所放出的热量为_____kJ。
CO2(g)+H2(g) ΔH=-41.1kJ·mol-1,则CO2与H2反应合成CH3OH(g)的热化学方程式为_______________,反应在10 min内所放出的热量为_____kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语在化学学科中作用非常重要,以下有关化学用语描述正确的是( )
A.Mg2+的电子排布式:1s22s22p63s2
B.氨气的空间结构:三角形
C.Na2S的电子式:![]()
D.甲醛的结构简式:CH2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com