
| A. | 偏高 | B. | 偏低 | C. | 准确 | D. | 无法判断 |
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取少量完全分解的固体产物于试管中,加入稀盐酸 | 若有淡黄色沉淀,则有Na2S2O3存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
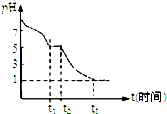
| A. | 加入盐酸的体积大于10 mL | B. | c(NH4+)=c(Cl-) | ||
| C. | 加入盐酸的体积等于10 mL | D. | c(NH4+)<c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<b | B. | a=b | ||
| C. | 水的离子积为1.0×10-(7+a) | D. | 水的离子积为1.0×10-(b+a) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,电子通过外电路从正极流向负极 | |
| B. | 负极的电极反应式为Zn+4OH--2e-═ZnO22-+2H2O | |
| C. | 该电池每消耗65 g Zn吸收11.2 LO2 | |
| D. | 在电池工作过程中,电解液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 催化剂只改变反应的正反应速率 | |
| B. | 催化剂通过升高反应的活化能来加快反应速率 | |
| C. | 催化剂能够改变反应的反应热 | |
| D. | 催化剂不能改变反应物的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
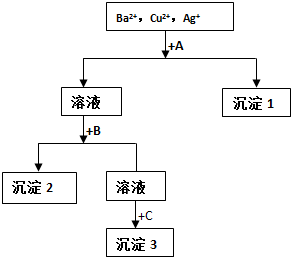
| A. | 试剂A只能为盐酸溶液 | |
| B. | 沉淀2可能是BaSO4 也可能是Cu(OH)2 | |
| C. | 每加一种试剂需过量且要过滤后方可进行下一步 | |
| D. | 生成沉淀1的离子方程式可能为:Cu2++2OH-=Cu(OH)2↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com