
“―÷ΣKsp(AgCl)=1.8ΓΝ10-10Θ§Ksp(AgI)=1.0ΓΝ10-16ΓΘœ¬Ν–ΙΊ”ΎΡ―»ήΈο÷°ΦδΉΣΜ·ΒΡΥΒΖ®÷–¥μΈσΒΡ «( )
| AΘ°AgCl≤Μ»ή”ΎΥ°Θ§≤ΜΡήΉΣΜ·ΈΣAgI |
| BΘ°ΝΫ÷÷Ρ―»ήΈοΒΡKspœύ≤ν‘Ϋ¥σΘ§Ρ―»ήΈοΨΆ‘Ϋ»ί“ΉΉΣΜ·ΈΣΗϋΡ―»ήΒΡΈο÷ |
| CΘ°AgI±»AgClΗϋΡ―»ή”ΎΥ°Θ§Υυ“‘AgClΩ…“‘ΉΣΜ·ΈΣAgI |
DΘ°≥ΘΈ¬œ¬Θ§AgCl»τ“Σ‘ΎNaI»ή“Κ÷–ΩΣ ΦΉΣΜ·ΈΣAgIΘ§‘ρNaIΒΡ≈®Ε»±Ί–κ≤ΜΒΆ”Ύ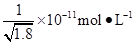 |

| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
≥ΘΈ¬œ¬Θ§œ¬Ν–”–ΙΊ¥ΉΥα»ή“ΚΒΡ–π ω÷–≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
| AΘ°pHΘΫ5.6ΒΡCH3COOH”κCH3COONaΜλΚœ»ή“Κ÷–ΘΚc(NaΘΪ)ΘΦc(CH3COOΘ≠) |
| BΘ°≈®Ε»ΨυΈΣ0.1 molΓΛLΘ≠1ΒΡCH3COOHΚΆCH3COONa»ή“ΚΒ»ΧεΜΐΜλΚœΚσΘΚc(CH3COOΘ≠)Θ≠c(CH3COOH)ΘΫ2[c(HΘΪ)Θ≠c(OHΘ≠)] |
| CΘ°ΫΪpHΘΫaΒΡ¥ΉΥαœΓ ΆΈΣpHΘΫaΘΪ1ΒΡΙΐ≥Χ÷–Θ§c(CH3COOH)/c(HΘΪ)Φθ–Γ |
| DΘ°Β»ΧεΜΐpHΘΫaΒΡ¥ΉΥα”κpHΘΫbΒΡNaOH»ή“Κ«ΓΚΟ÷–ΚΆ ±Θ§aΘΪbΘΫ14 |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
≥ΘΈ¬œ¬Θ§ΫΪ“ΜΕ®≈®Ε»ΒΡ―ΈΥαΚΆ¥ΉΥαΦ”Υ°œΓ ΆΘ§»ή“ΚΒΡΒΦΒγΡήΝΠΥφ»ή“ΚΧεΜΐ±δΜ·ΒΡ«ζœΏ»γΆΦΥυ ΨΓΘ≈–Εœœ¬Ν–ΥΒΖ®÷–Θ§’ΐ»ΖΒΡ «Θ® Θ©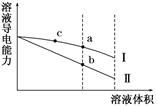
| AΘ°ΝΫ»ή“ΚœΓ Ά«ΑΒΡ≈®Ε»œύΆ§ |
| BΘ°aΓΔbΓΔc»ΐΒψ»ή“ΚΒΡpH”…¥σΒΫ–ΓΥ≥–ρΈΣaΘΨbΘΨc |
| CΘ°aΒψΒΡKW÷Β±»bΒψΒΡKW÷Β¥σ |
| DΘ°aΒψΥ°ΒγάκΒΡc(HΘΪ)¥σ”ΎcΒψΥ°ΒγάκΒΡc(HΘΪ) |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
»ΥΧε―Σ“Κάο¥φ‘Ύ÷Ί“ΣΒΡΥαΦνΤΫΚβΘΚ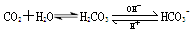 Θ§ Ι»ΥΧε―Σ“ΚpH±Θ≥÷‘Ύ7.35ΓΪ7.45Θ§Ζώ‘ρΨΆΜαΖΔ…ζΥα÷–ΕΨΜρΦν÷–ΕΨΓΘΤδpHΥφc(HCO3-)ΓΟc(H2CO3)±δΜ·ΙΊœΒ»γœ¬±μΘΚ
Θ§ Ι»ΥΧε―Σ“ΚpH±Θ≥÷‘Ύ7.35ΓΪ7.45Θ§Ζώ‘ρΨΆΜαΖΔ…ζΥα÷–ΕΨΜρΦν÷–ΕΨΓΘΤδpHΥφc(HCO3-)ΓΟc(H2CO3)±δΜ·ΙΊœΒ»γœ¬±μΘΚ
| c(HCO3-)ΘΚc(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
“―÷Σ25Γφ ±Θ§CaSO4‘ΎΥ°÷–ΒΡ≥ΝΒμ»ήΫβΤΫΚβ«ζœΏ»γΆΦΥυ ΨΘ§œρ100 mLΗΟΧθΦΰœ¬ΒΡCaSO4±ΞΚΆ»ή“Κ÷–Φ”»κ400 mL 0.01 molΓΛLΘ≠1Na2SO4»ή“ΚΘ§’κΕ‘¥ΥΙΐ≥ΧΒΡœ¬Ν––π ω’ΐ»ΖΒΡ «(ΓΓΓΓ)
| AΘ°»ή“Κ÷–Έω≥ωCaSO4≥ΝΒμΘ§Ήν÷’»ή“Κ÷–c(SO42ΓΣ)Ϋœ‘≠ά¥ΒΡ¥σ |
| BΘ°»ή“Κ÷–Έό≥ΝΒμΈω≥ωΘ§»ή“Κ÷–c(Ca2ΘΪ)ΓΔc(SO42ΓΣ)ΕΦ±δ–Γ |
| CΘ°»ή“Κ÷–Έω≥ωCaSO4≥ΝΒμΘ§»ή“Κ÷–c(Ca2ΘΪ)ΓΔc(SO42ΓΣ)ΕΦ±δ–Γ |
| DΘ°»ή“Κ÷–Έό≥ΝΒμΈω≥ωΘ§ΒΪΉν÷’»ή“Κ÷–c(SO42ΓΣ)Ϋœ‘≠ά¥ΒΡ¥σ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
œρ50 mL 0.018 molΓΛL-1 AgNO3»ή“Κ÷–Φ”»κ50 mL 0.02 molΓΛLΘ≠1―ΈΥαΓΘ“―÷ΣAgCl(s)ΒΡ»ήΕ»Μΐ≥Θ ΐKsp= 1ΓΝ10Θ≠10Θ§ΜλΚœΚσ»ή“ΚΒΡΧεΜΐ±δΜ·Κω¬‘≤ΜΦΤΓΘœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «( )
| AΘ°ΜλΚœΚσΘ§»ή“Κ÷–ΩœΕ®”–≥ΝΒμ…ζ≥… |
| BΘ°≥ΝΒμ…ζ≥…Κσ»ή“Κ÷–Ag+ΒΡ≈®Ε»ΈΣ10-5 molΓΛL-1 |
| CΘ°≥ΝΒμ…ζ≥…Κσ»ή“ΚΒΡpHΘΫ2 |
| DΘ°ΜλΚœΚσΘ§…ΐΗΏΈ¬Ε»Θ§»ή“Κ÷–Ag+ΒΡ≈®Ε»‘ω¥σ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
‘Ύ0.1 mol/LΒΡ¥ΉΥαΡΤ»ή“Κ÷–Φ”»κΒ»ΧεΜΐΒΡœ¬Ν–Έο÷ Θ§»ή“Κ÷–άκΉ”≈®Ε»¥σ–ΓΙΊœΒ’ΐ»ΖΒΡ «( )
| AΘ°Υ°ΘΜc(CH3COO-)ΘΨc(Na+)ΘΨc(OH-)ΘΨc(H+) |
| BΘ°0.1 mol/L―ΈΥαΘΜc(Na+)=c(Cl-)ΘΨc(H+)ΘΨc(CH3COO-)ΘΨc(OH-) |
| CΘ°0.1 mol/L¥ΉΥαΘΜc(Na+)ΘΨc(CH3COO-)ΘΨc(H+)ΘΨc(OH-) |
| DΘ°0.1 mol/L«β―θΜ·ΡΤΘΜc(Na+)ΘΨc(CH3COO-)ΘΨc(OH-)ΘΨc(H+) |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
ΦΉΥαΒΡœ¬Ν––‘÷ ÷–Θ§Ω…“‘÷ΛΟςΥϋ «»θΒγΫβ÷ ΒΡ «( )
| AΘ°1 mol / LΦΉΥα»ή“ΚΒΡc(H+)="0.01" mol/L |
| BΘ°ΦΉΥαΡή”κΥ°“‘»ΈΚΈ±»άΐΜΞ»ή |
| CΘ°10 mL 1 mol/LΦΉΥα«ΓΚΟ”κ10 mL 1 mol/L NaOH»ή“ΚΆξ»ΪΖ¥”Π |
| DΘ°ΦΉΥα»ή“ΚΒΡΒΦΒγ–‘±»―ΈΥαΒΡ»θ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΒΞ―ΓΧβ
25 Γφ ±Θ§≈®Ε»ΨυΈΣ0.1 molΓΛLΘ≠1ΒΡHA»ή“ΚΚΆBOH»ή“ΚΘ§pHΖ÷±π «1ΚΆ11ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «(ΓΓΓΓ)
| AΘ°‘Ύ0.1 molΓΛLΘ≠1BA»ή“Κ÷–Θ§c(AΘ≠)ΘΪc(HΘΪ)ΘΫc(BOH)ΘΪc(BΘΪ) |
| BΘ°»τΫΪ0.1 molΓΛLΘ≠1 BOH»ή“ΚœΓ Ά÷Ν0.001 molΓΛLΘ≠1‘ρ»ή“ΚΒΡpHΘΫ9 |
| CΘ°»τΫΪ“ΜΕ®ΝΩΒΡ…œ ωΝΫ»ή“ΚΜλΚœΚσpHΘΫ7Θ§‘ρΜλΚœ“Κ÷–ΘΚc(AΘ≠)>c(BΘΪ) |
| DΘ°»τΫΪ…œ ωΝΫ»ή“ΚΑ¥ΧεΜΐ±»1ΓΟ1ΜλΚœΘ§‘ρΜλΚœ“Κ÷–ΘΚc(AΘ≠)>c(BΘΪ)>c(HΘΪ)>c(OHΘ≠) |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com