
下列离子方程式式书写正确的是
A.向偏铝酸钠溶液中滴加碳酸氢钠溶液:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
B.Fe(NO3)3溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+
C.酸性KMnO4溶液与H2O2反应证明H2O2具有还原性:MnO4-+10H++H2O2=2Mn2++6H2O
D.澄清的石灰水中加入过量的NaHCO3溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上适应性考试二化学试卷(解析版) 题型:填空题
二水合重重铬酸钠(Na2Cr2O7.2H2O),[已知M(Na2Cr2O7.2H2O)=298g/mol]俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO.Cr2O3,还含有A1203、MgO、Si02等杂质)为主要原料生产,其主要工艺流程如图:
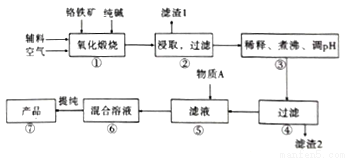
已知信息:
Ⅰ.“①”中涉及的主要反应是:4FeO·Cr2O3+8Na2CO3+7O2=8Na2CrO4+2Fe2O3+8CO2
Ⅱ.部分阳离子以氢氧化物形式完全沉淀时溶液的PH如下:
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
完全沉淀时溶液PH | 4.7 | 3.7 | 11.2 | 5.6 |
(1).杂质A12O3、SiO2与纯碱反应转变为可溶性盐,写出A12O3纯碱反应的化学方程式为:______________,滤渣1的主要成分为__________________。
(2).“③”中通过调节PH除去杂质,调节PH至___________。
(3).“⑤”中向滤液中加入物质A,得到Na2Cr2O3和Na2SO4的混合溶液,物质A为__________,简述原因:______________________________。(用离子方程式及文字加以说明)
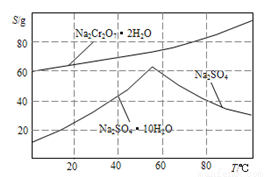
(4).如图是Na2Cr2O3.2H2O和Na2SO4的溶解度曲线。提纯的实验操作:将Na2Cr2O3和Na2SO4的混合溶液______________________,得到Na2SO4固体和较纯净的Na2Cr2O3溶液。
(5).实验室测定所得产品中红矾钠的纯度,称取产品3.2g,配成250mol溶液,取出25.00mL于锥形瓶中,加入10mL2mol/LH2SO4和足量碘化钾,放于暗处5min,写出离子方程式:________________。然后加水100mL,加入3mL淀粉指示剂,用0.1000mol/LNa2S2O3标准溶液滴定I2+2S2O32-=2I-+S4O62-若达到滴定终点时,共用去Na2S2O3标准溶液60mL,所得产品的纯度是_________(结果保留小数点后1位)。
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:推断题
Ⅰ、下列转化关系中,X、Y是生活中生活中用途广泛的两种金属单质,A、B是氧化物,A呈红棕色,C、D、E是中学常见的三种化合物。分析转化关系回答问题:
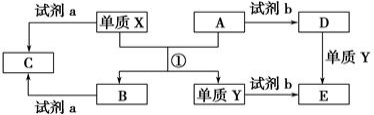
(1)请写出反应①的化学方程式_____________________。
(2)试剂a是_________溶液(写一种即可)
(3)若试剂b是H 2 SO 4 ,工业上用E、H 2 SO 4 和NaNO 2 为原料制取高效净水剂Y(OH)SO 4 ,已知还原产物为NO,则该反应的化学方程式是________________________。
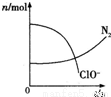
Ⅱ、(1)某容器中发生了一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种粒子,在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.
该反应的离子方程式是___________________。
(2)氮氧化合物是大气污染的重要盐因素,将NOx转化为无害物质是当前研究的重要课题。
①下式中X必须为无污染的物质,系数n可以为0。
NO2+G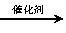 N2+H2O+nX(未配平的反应式)。
N2+H2O+nX(未配平的反应式)。
下列化合物中,满足上述反应式中的G是________(填写字母)。
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
② 若G为天然气的主要成分,则X为____________,n=__________。
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
下列说法正确的是
①氢氧化铝具有弱碱性,可用于制胃酸中和剂
②铝罐可久盛食醋
③FeCl3溶液可用于铜质印刷线路板制作,该反应是置换反应
④ 将水蒸气通过灼热的铁粉,出现的现象是粉末变红,说明铁与水在高温下发生反应
⑤明矾能水解生成Al(OH)3.胶体,可用作净水剂
⑥Fe与S混合加热生成FeS2
⑦Fe与稀硝酸、稀硫酸反应均有气泡产生,说明Fe与两种酸均发生置换反应
⑧氧化铁能与酸反应,因而可利用于制作红色涂料
A. 1个 B. 2个 C. 3个 D. 5个
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
下列溶液配制实验的描述完全正确的是
A. 在容量瓶中先加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸
B. 用浓盐酸配制1 : 1(体积比)的稀盐酸(约6mol.L-1)通常需要用容量瓶等仪器
C. 配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4以防水解
D. 用pH=1的盐酸配制100mL、pH ="2" 的盐酸所需全部玻璃仪器有100mL容量瓶、烧杯、玻璃棒、胶头滴管
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期期中化学试卷(解析版) 题型:选择题
下列有关实验的说法正确的是
A.除去铁粉中混有少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
B.光照氯水有气泡冒出,该气体主要为Cl2
C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D.Na[Al(OH)4]溶液和盐酸可以通过相互滴加的方法来鉴别,NaHCO3溶液和Ca(OH)2溶液也可以通过相互滴加的方法来鉴别
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com