
���� ��1��ͬ��ͬѹ�£��������ʵ���֮�ȵ����������֮�ȣ�������Ŀ֮�ȵ������ʵ���֮�ȣ�����m=nM��������֮�ȣ�
��2�����������غ����F���������ٸ���n=$\frac{m}{M}$����F�����ʵ���������V=nVm����F�������
��3��A�Ƕ��۽�������������ΪA��NO3��2�����ݸ������εĻ�ѧʽ������������ε����ʵ�����Ȼ�����M=$\frac{m}{n}$������������ε�Ħ��������
��4���ȼ����ϡ��ǰ��������ӵ�Ũ�ȣ�Ȼ�����ϡ��������������ӵ����ʵ���������㣮
��� �⣺��1��ͬ��ͬѹ�£��������ʵ���֮�ȵ����������֮�ȣ���������CO2��H2�����ʵ���֮����1�����3���=1��3��
CO2��H2��������ķ�����Ŀ��ȣ���������ʵ�����ȣ�����m=nM��֪����������֮��Ϊ44g/mol��2g/mol=22��1��
�ʴ�Ϊ��1��3��22��1��
��2�����������غ㶨�ɣ�����F������Ϊ44g+49g-76g=17g��F��������ʵ���Ϊ��$\frac{17g}{34g/mol}$=0.5mol�������F�����Ϊ0.5mol��22.4L/mol=11.2L��
�ʴ�Ϊ��11.2L��
��3��A�Ƕ��۽�������������ΪA��NO3��2��6.02��1023����������ӵ����ʵ���Ϊ��$\frac{6.02��1{0}^{23}}{6.02��1{0}^{23}mo{l}^{-1}}$=1mol����n��A��NO3��2��=$\frac{1}{2}$n��NO3-��=0.5mol���������ε�Ħ������Ϊ��$\frac{84g}{0.5mol}$=164 g•mol-1��
�ʴ�Ϊ��164 g•mol-1��
��4��5mol/L��Mg��NO3��2��Һ����������ӵ�Ũ��Ϊ��5mol/L��2=10mol/L����a mL����Һϡ����b mL��ϡ��������������ӵ����ʵ������䣬ϡ�ͺ���Һ��NO3-�����ʵ���Ũ���ǣ�$\frac{10mol/L��a��1{0}^{-3}L}{b��1{0}^{-3}L}$=$\frac{10a}{b}$mol/L��
�ʴ�Ϊ��$\frac{10a}{b}$mol/L��
���� ���⿼�������ʵ����ļ��㣬��Ŀ�Ѷ��еȣ���ȷ���ʵ�����Ħ������������Ħ�����������٤������֮��Ĺ�ϵ���ɽ������֪ʶ��϶࣬��ֿ�����ѧ���ķ�����������ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
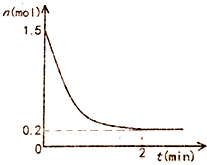 ��һ����̶�Ϊ10L���ܱպ��������г���1.5mol������������Ӧ��2NH3��g��?N2��g��+3H2��g����H=93KJ/mol��Ӧ������NH3���ʵ�����ʱ��ı仯��ͼ��ʾ��
��һ����̶�Ϊ10L���ܱպ��������г���1.5mol������������Ӧ��2NH3��g��?N2��g��+3H2��g����H=93KJ/mol��Ӧ������NH3���ʵ�����ʱ��ı仯��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ������������Һ��Ӧ�����ӷ���ʽΪH++OH-=H2O | |
| B�� | H2S��ˮ��Һ�еĵ��룺H2S+H2O?H3O++HS- | |
| C�� | �����ȼ����Ϊ890.3 kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O ��g����H=-890.3 kJ•mol-1 | |
| D�� | ˫��ˮ�м���ϡ�����KI��Һ��H2O2+2I-+H+�TI2+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100mL 0.5 mol/L MgCl2��Һ | B�� | 200mL 0.25 mol/L KCl��Һ | ||
| C�� | 100mL 0.5 mol/L HCl��Һ | D�� | 100mL 0.5 mol/L NaClO��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ܵ�����Ǣܢޢ� | |
| B�� | �����������ڵ���ʵ��Ǣ٢ڢۢܢ��� | |
| C�� | ���ڷǵ���ʵ��Ǣڢݢ� | |
| D�� | ���������У�����ˮ�ܹ�����������Ǣ٢ڢܢݢߢ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ƿ���������θ����� | |
| B�� | �������ֿ���������ʳƷ������ | |
| C�� | ˮ�������ݹ���ľ�ļ��ܷ��������ͻ� | |
| D�� | Si����������ά |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
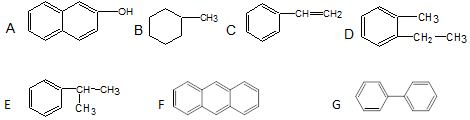
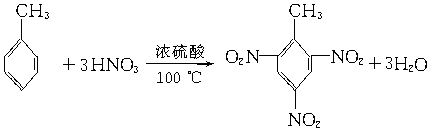 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ʵ������ | �� �� |
| A | �ⶨ��Ũ�ȵ�Na2CO3��Na2SO3��Һ��pH | ǰ��pH�Ⱥ��ߵĴ� | �ǽ����ԣ�S��C |
| B | ��������NaOH��Һ���Ⱥ���AgNO3��Һ | δ���ֵ���ɫ���� | ������û��ˮ�� |
| C | ���Ũ�ȵ�KCl��KI���Һ�еμ�AgNO3��Һ | �ȳ��ֻ�ɫ���� | Ksp��AgCl����Ksp��AgI�� |
| D | ��KI��FeCl3��Һ���Թ��л�Ϻ���CCl4�������� | �²�Һ�����Ϻ�ɫ | �����ԣ�Fe3+��I2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ�����ϵڶ���ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A�����ᡢ��������ƺ���ʯ�ҷֱ������ᡢ��κ�������
B���ƾ������ᱵ��ˮ�ֱ����ڵ���ʡ�ǿ����ʺ��������
C������������������ɢϵ�ı��������Ǿ��ж��������
D�����ð�Ĥ�ɳ�ȥ������Һ�е�����NaCl
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com