
下列对四个量子数的说法正确的是( )
A.自旋磁量子数ms用来标记电子的自旋运动状态
B.磁量子数m=0的轨道都是球形的轨道
C.角量子数l的可能取值是从0到n-1的整数
D.多电子原子中,电子的能量只取决于主量子数n
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
如图是一种航天器能量储存系统原理示意图。下列说法正确的是( )
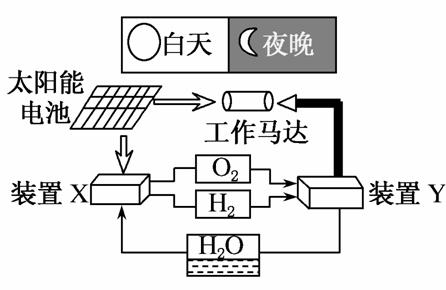
A.该系统中只存在3种形式的能量转化
B.装置Y中负极的电极反应式为:O2+2H2O+4e-===4OH-
C.装置X能实现燃料电池的燃料和氧化剂再生
D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)A、B、C、D、E、F是元素周期表前四周期的元素,它们在元素周期表中的位置如图所示:
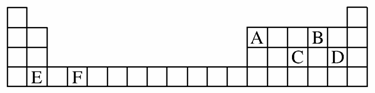
①写出F的基态原子的核外电子排布式:___________________________________________
________________________________________。
②C元素的第一电离能比同周期相邻的两种元素的第一电离能都高的原因是____________________。
(2)A、B、C 3种元素中,A的第一电离能最小,C的电负性最大,3种元素的失电子能力由强到弱的顺序为
___________________________________________。
(3)D、E两种元素形成的化合物化学式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有________种,金属性最强的元素最高价氧化物的水化物是________(填化学式)。
(2)属于稀有气体的是________(填元素符号,下同)。
(3)第3周期中,原子半径最大的是(稀有气体除外)________。
(4)推测Si、N最简单氢化物的稳定性________大于________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的原子序数为29,请填写下列空白:
(1)该元素原子的核外电子总数是________。
(2)该元素共有________个电子层,________个能级。
(3)写出它的价电子排布式____________,价电子轨道表示式__________________。
(4)该元素在同周期表中位于第________周期________族。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液电解一段时间后,再加入相关物质,溶液能恢复原状况的是( )
| 选项 | 电解质溶液 | 阳极 | 阴极 | 加入的物质 |
| A | NaCl溶液 | 碳 | 铁 | 盐酸 |
| B | NaOH溶液 | 碳 | 碳 | 水 |
| C | 硫酸铜溶液 | 碳 | 碳 | 硫酸铜 |
| D | 硫酸 | 铁 | 碳 | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、空间电视转播站、飞机、轮船、电脑、收音机、照相机、电子手表、心脏起搏器等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
(1)电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O===2Ag+Zn(OH)2。
①工作时电流从________极流向________极(填“Ag2O”或“Zn”)。
②电极反应式:正极______________________________,
负极:_____________________________________________。
③工作时电池正极区的pH________(填“增大”“减小”或“不变”)。
(2)氢镍电池是近年来开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应式是H2+NiO(OH)放电充电Ni(OH)2。
电池放电时,负极是________,负极的电极反应式为________,正极的电极反应式为____________________,正极附近溶液的pH如何变化?________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com