
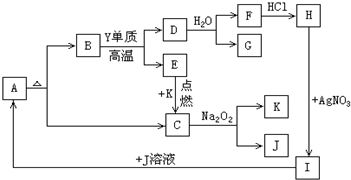
·ÖĪö CŹĒĘųĢ壬ÄÜÓė¹żŃõ»ÆÄĘ·“Ӧɜ³ÉĘųĢåKŗĶĪļÖŹJ£¬ŌņæÉÖŖCĪŖCO2£¬KĪŖO2£¬JĪŖNa2CO3£¬ĘųĢåEŌŚŃõĘųÖŠµćČ¼Éś³ÉCO2£¬ĖłŅŌEĪŖCO£¬·Ē½šŹōµ„ÖŹYÓėBŌŚøßĪĀĻĀ·“Ӧɜ³ÉDŗĶE£¬ŌņYÓ¦ĪŖC£¬BĪŖÓ¦ĪŖ¶ž¼Ū½šŹōŌŖĖŲXµÄ»ÆŗĻĪļ£¬øł¾ŻAŹÜČČ·Ö½āÉś³ÉBŗĶ¶žŃõ»ÆĢ¼£¬æÉÖŖAĪŖCaCO3£¬BĪŖCaO£¬CaOÓėĢ¼·“Ӧɜ³ÉDĪŖCaC2£¬CaC2ÓėĖ®·“Ӧɜ³ÉFĪŖCa£ØOH£©2£¬ĘųĢåGĪŖC2H2£¬FÓėĀČ»ÆĒā·“Ӧɜ³ÉHĪŖCaCl2£¬CaCl2ÓėĻõĖįŅų·“Ӧɜ³ÉIĪŖCa£ØNO3£©2£¬IÓėNa2CO3·“Ӧɜ³ÉĢ¼ĖįøĘ£¬·ūŗĻø÷ĪļÖŹµÄ×Ŗ»Æ¹ŲĻµ£¬¾Ż“Ė“šĢā£»
½ā“š ½ā£ŗCŹĒĘųĢ壬ÄÜÓė¹żŃõ»ÆÄĘ·“Ӧɜ³ÉĘųĢåKŗĶĪļÖŹJ£¬ŌņæÉÖŖCĪŖCO2£¬KĪŖO2£¬JĪŖNa2CO3£¬ĘųĢåEŌŚŃõĘųÖŠµćČ¼Éś³ÉCO2£¬ĖłŅŌEĪŖCO£¬·Ē½šŹōµ„ÖŹYÓėBŌŚøßĪĀĻĀ·“Ӧɜ³ÉDŗĶE£¬ŌņYÓ¦ĪŖC£¬BĪŖÓ¦ĪŖ¶ž¼Ū½šŹōŌŖĖŲXµÄ»ÆŗĻĪļ£¬øł¾ŻAŹÜČČ·Ö½āÉś³ÉBŗĶ¶žŃõ»ÆĢ¼£¬æÉÖŖAĪŖCaCO3£¬BĪŖCaO£¬CaOÓėĢ¼·“Ӧɜ³ÉDĪŖCaC2£¬CaC2ÓėĖ®·“Ӧɜ³ÉFĪŖCa£ØOH£©2£¬ĘųĢåGĪŖC2H2£¬FÓėĀČ»ÆĒā·“Ӧɜ³ÉHĪŖCaCl2£¬CaCl2ÓėĻõĖįŅų·“Ӧɜ³ÉIĪŖCa£ØNO3£©2£¬IÓėNa2CO3·“Ӧɜ³ÉĢ¼ĖįøĘ£¬·ūŗĻø÷ĪļÖŹµÄ×Ŗ»Æ¹ŲĻµ£¬
£Ø1£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬ŌŖĖŲXĪŖCa£¬ŌŖĖŲYµÄĆū³ĘĪŖĢ¼£¬
¹Ź“š°øĪŖ£ŗCa£»Ģ¼£»
£Ø2£©CaC2ÓėĖ®·“Ӧɜ³ÉCa£ØOH£©2ŗĶC2H2£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCaC2+2H2O”śC2H2”ü+Ca£ØOH£©2£¬
¹Ź“š°øĪŖ£ŗCaC2+2H2O”śC2H2”ü+Ca£ØOH£©2£»
£Ø3£©·“Ó¦C”śK+JĪŖ¶žŃõ»ÆĢ¼Óė¹żŃõ»ÆÄĘ·“Ӧɜ³ÉŃõĘųŗĶĢ¼ĖįÄĘ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2CO2+2Na2O2=2Na2CO3+O2£¬
¹Ź“š°øĪŖ£ŗ2CO2+2Na2O2=2Na2CO3+O2£»
£Ø4£©JĪŖNa2CO3£¬ÄÜÓėCaO”¢Ca£ØOH£©2”¢CaCl2µČ·“Ӧɜ³ÉCaCO3£¬
¹Ź“š°øĪŖ£ŗB”¢F”¢H£»
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļĶʶĻ£¬Éę¼°C”¢NaŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬ĪļÖŹµÄŠŌÖŹ¼°Ļą»„×Ŗ»Æ¹ŲĻµŹĒĶʶĻĶ»ĘĘæŚ£¬ĢāÄæ×ŪŗĻŠŌ½ĻĒ棬ÄѶČÖŠµČ£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬¶Ōѧɜ×ŪŗĻĖ¼Ī¬ÄÜĮ¦ŅŖĒó½Ļøߣ®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Mg2+µÄ½į¹¹Ź¾ŅāĶ¼£ŗ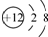 | |
| B£® | ĘĻĢŃĢĒµÄ½į¹¹¼ņŹ½£ŗC6H12O6 | |
| C£® | H2O2µÄµē×ÓŹ½£ŗ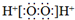 | |
| D£® | ĮņĖįµÄµēĄė·½³ĢŹ½£ŗH2SO4ØTH22++SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
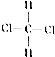 ŗĶ
ŗĶ ¢ąŅŅĶéŗĶĪģĶé
¢ąŅŅĶéŗĶĪģĶé²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1ÖÖ | B£® | 2ÖÖ | C£® | 3ÖÖ | D£® | 4ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓŠ5.6 g½šŹō±»øÆŹ“ | B£® | ÓŠ6.5 g½šŹō±»Ńõ»Æ | ||
| C£® | ÓŠ0.15 mol½šŹōŹ§Č„µē×Ó | D£® | ±ź×¼×“æöĻĀÓŠ4.48 L H2ŅŻ³ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

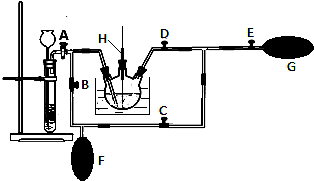
| ŹµŃ鱹ŗÅ | ŹŌ¹ÜaÖŠŹŌ¼Į | ŹŌ¹ÜbÖŠŹŌ¼Į | ²āµĆÓŠ»ś²ćµÄŗń¶Č/cm |
| A | 3mLŅŅ“¼”¢2mLŅŅĖį”¢1mL18mol•L-1 ÅØĮņĖį | ±„ŗĶNa2CO3ČÜŅŗ | 5.0 |
| B | 3mLŅŅ“¼”¢2mLŅŅĖį | 0.1 | |
| C | 3mLŅŅ“¼”¢2mLŅŅĖį”¢6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mLŅŅ“¼”¢2mLŅŅĖį”¢ŃĪĖį | 1.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
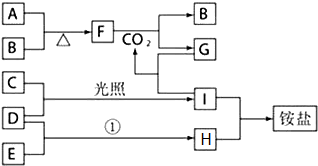 ijŠĖȤŠ”×éµÄĶ¬Ń§·¢ĻÖ”¶øßÖŠ»Æѧ£Ø±ŲŠŽ1£©”·ÖŠŃ§Ļ°µÄµ„ÖŹ¼°Ęä»ÆŗĻĪļ£Ø»ņĘäČÜŅŗ£©“ęŌŚČēĶ¼µÄ×Ŗ»Æ¹ŲĻµ£¬ŅŃÖŖB”¢C”¢D”¢EŹĒ·Ē½šŹōµ„ÖŹ£¬ĒŅŌŚ³£ĪĀ³£Ń¹ĻĀ¶¼ŹĒĘųĢ壻FĪŖµ»ĘÉ«·ŪÄ©£¬»ÆŗĻĪļHŗĶIĶس£×“æöĻĀ³ŹĘųĢ壻·“Ó¦¢ŁŹĒ»Æ¹¤Éś²śÖŠµÄŅ»ÖÖÖŲŅŖ¹ĢµŖ·“Ó¦£®
ijŠĖȤŠ”×éµÄĶ¬Ń§·¢ĻÖ”¶øßÖŠ»Æѧ£Ø±ŲŠŽ1£©”·ÖŠŃ§Ļ°µÄµ„ÖŹ¼°Ęä»ÆŗĻĪļ£Ø»ņĘäČÜŅŗ£©“ęŌŚČēĶ¼µÄ×Ŗ»Æ¹ŲĻµ£¬ŅŃÖŖB”¢C”¢D”¢EŹĒ·Ē½šŹōµ„ÖŹ£¬ĒŅŌŚ³£ĪĀ³£Ń¹ĻĀ¶¼ŹĒĘųĢ壻FĪŖµ»ĘÉ«·ŪÄ©£¬»ÆŗĻĪļHŗĶIĶس£×“æöĻĀ³ŹĘųĢ壻·“Ó¦¢ŁŹĒ»Æ¹¤Éś²śÖŠµÄŅ»ÖÖÖŲŅŖ¹ĢµŖ·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½µµĶĪĀ¶Č | B£® | Ōö“óŃ¹Ēæ | C£® | ³äČėŅ»¶ØĮæCO2 | D£® | ŌŁ¼ÓČėŅ»Š©Ģś·Ū |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com