
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
A、该反应的化学方程式为CO+H2O
| |||
| B、恒温恒容下,增大压强,H2浓度一定减小 | |||
| C、升高温度,正反应速率增大,逆反应速率减小 | |||
| D、该反应的焓变为正值 |
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
A、 如图实验制取少量的Fe(OH)3胶体 |
B、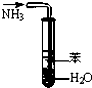 如图实验试管中溶液吸收NH3,并防止倒吸 |
C、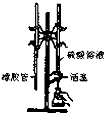 如图实验用H2SO4标准溶液滴定NaOH溶液 |
D、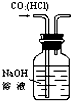 可用如图实验装置除去CO2气体中含有的少量HCl杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH由小到大的顺序是①<②<③<④ |
| B、溶液中水电离出的H+浓度由小到大的顺序是②<①<④<③ |
| C、取一定体积的④溶液,分别和①、②、③溶液完全中和,消耗①、②、③溶液的体积由小到大的顺序是②<①<③ |
| D、取a体积的①溶液和b体积的④溶液混合后,溶液的pH为3,则a:b约为11:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na,Mg,Al金属性依次减弱 |
| B、HCl,H2S,PH3稳定性依次减弱 |
| C、NaOH,KOH,CsOH碱性依次减弱 |
| D、S2-,Cl-,Ca2+半径依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在蒸馏水中滴加浓H2SO4或者Na2CO3溶液,KW均不变 |
| B、向某氨水中加入一定浓度的稀硫酸至溶液呈中性,混合溶液中离子存在关系式: c(SO42-)=c(NH4+)>c(H+)=c(OH-) |
| C、NaCl 溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| D、在Na2S 稀溶液中,c(H+)<c(OH-)-c(H2S)-c(HS-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
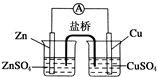
| A、锌电极发生还原反应,铜电极发生氧化反应 |
| B、盐桥中的阴离子向硫酸铜溶液中迁移 |
| C、电子从锌电极通过电流计流向铜电极 |
| D、铜电极上发生的电极反应为2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4 | B、4.5 | C、5 | D、5.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com