
| 实验序号 | 催化剂(1g) | … | |||
| 1 | α-Fe2O3 | ||||
| 2 | γ-Fe2O3 | ||||
| 3 | MnO2 | ||||
| ﹕ ﹕ |
| 实验 编号 | 催化剂 | 反应时间和生成m(O2)/g | |||||
| 10s | 20s | 30s | 40s | 50s | 60s | ||
| 1 | α-Fe2O3 | ||||||
| 2 | γ-Fe2O3 | ||||||
| 3 | MnO2 | ||||||
| 实验 编号 | 催化剂 | 反应时间和m(O2)/g | |||||
| 10s | 20s | 30s | 40s | 50s | 60s | ||
| 1 | α-Fe2O3 | ||||||
| 2 | γ-Fe2O3 | ||||||
| 3 | MnO2 | ||||||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、标准状况下,含有NA个氦原子的氦气的体积约为11.2L |
| B、标准状况下,44.8L H2O的分子数为2NA |
| C、常温常压下,22g CO2含有原子总数为1.5NA |
| D、含有1mol HCl 的稀盐酸与足量的铁发生反应,转移的电子总数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸\反应进程\ | 1min | 2 min | 3 min | 4 min | 5 min |
| 3.0mol/L HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5 mol/L H2SO4 | 产生的气泡很少 | ||||
| 3.0mol/L H2SO4 | 产生的气泡很少 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
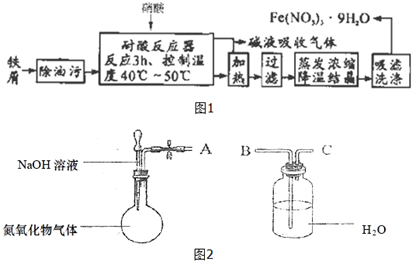
查看答案和解析>>
科目:高中化学 来源: 题型:
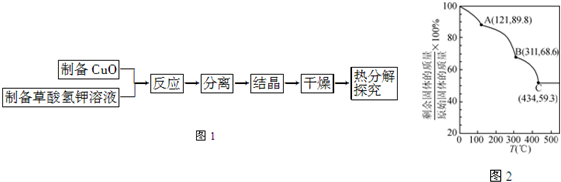
| ||
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
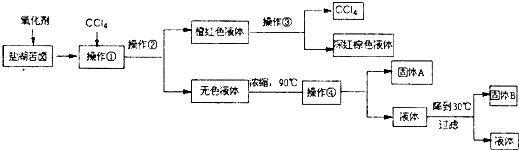

查看答案和解析>>
科目:高中化学 来源: 题型:

| 银盐 性质 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.34×10-6 | 7.1×10-7 | 1.1×10-8 | 6.5×10-5 | 1.0×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |
| B、煤经过气化和液化两个物理变化,可变为清洁能 |
| C、高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 |
| D、太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com