
【题目】己知木炭在一定条件下与浓硝酸反应生成两种+4价的氧化物。为了探究一氧化氮(NO)能否与过氧化钠反应,以及反应后的产物中是否有亚硝酸钠(NaNO2),某小组同学设计了如图所示装置(夹持仪器和连接用的乳胶管已经省略)。为了完成该实验,按气流方向A→E→C→B→D→尾气处理装置(略)顺序连接以下装置。请回答相关问题:
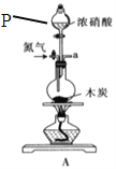
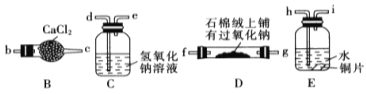
(1)仪器P的名称是 。
(2)写出浓硝酸与木炭反应的化学方程式 。
(3)检查气密性并装入药品后,要进行以下三项操作:a.点燃酒精灯,b.滴加浓硝酸,c.通入一段时间的氮气,则它们正确顺序是 (填字母编号)。反应开始时先通入氮气的主要目的是 。
(4)实验中装置C的作用是 。装置E中观察到的主要实验现象有 。
(5)某同学经查阅资料后发现亚硝酸是弱酸,性质不稳定,室温下易分解生成一氧化氮。装置D中充分反应后,设计实验证明D中是否有亚硝酸钠生成 。
【答案】(1)分液漏斗 (2)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
(3)c b a 排除装置内空气,防止氧气将NO氧化
(4)除去NO中混有的CO2(或CO2和NO2)
铜片逐渐溶解,溶液变蓝,有无色气泡冒出(或红棕色气体变为无色气体)
(5)取装置D中固体少量于试管中,加入适量稀硫酸,若有气泡冒出且在溶液上方变成红棕色,证明D中有亚硝酸钠生成
【解析】
试题分析:(1)根据仪器的特征,仪器P的名称为分液漏斗。
(2)装置A中是浓硝酸和碳加热发生反应,反应生成二氧化氮和二氧化碳和水,反应的化学方程式为C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O。
CO2↑+4NO2↑+2H2O。
(3)探究一氧化氮(NO)能否与过氧化钠反应,则需要将NO2转化为NO,同时除去CO2和水蒸气,所以正确的连接顺序是c b a ;由于装置中含有空气,能氧化NO为NO2,所以先通入氮气的主要目的是排除装置内空气,防止氧气将NO氧化。
(4)混合气体中含有CO2,CO2能与过氧化钠反应,所以装置C的作用是除去NO中混有的CO2(或CO2和NO2);NO2溶于水生成NO和硝酸,硝酸氧化单质铜生成硝酸铜、一氧化氮和水,所以观察到的实验现象是铜片逐渐溶解,溶液变蓝,有无色气泡冒出。
(5)由于亚硝酸是弱酸,性质不稳定,室温下易分解成一氧化氮,所以检验D中是否有亚硝酸钠生成的实验方案是取装置D中固体少量于试管中,加入适量稀硫酸,若有气泡冒出且在溶液上方变成红棕色,证明D中有亚硝酸钠生成。


科目:高中化学 来源: 题型:
【题目】下列离子组在指定溶液中一定能大量共存的是( )
A.使pH试纸呈蓝色的溶液中:I-、Cl-、NO3-、Cu2+
B.使酚酞呈深红色的溶液中:Na+、Cl- 、H+、NO3-
C.含大量Ag+ 的溶液中:K+、Na+、NO3-、SO42-
D.含大量OH- 的溶液中:CO32-、Cl-、F- 、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性
Ⅰ.实验室制备FeBr2
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管.e是两只耐高温的瓷皿,其中盛有细铁粉.
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁
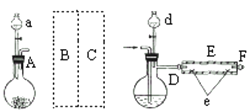
请回答:
(1)如何检查用塞子(插有导管和仪器)塞紧的D的气密性________.
(2)若在A中盛固体CaCO3,a中盛6mol/L盐酸,为使导入D中的CO2为干燥纯净的气体,则图中B、C处的装置和其中的试剂应是:B为________,C为________.为防止污染空气,实验时应在F处连接盛________的尾气吸收装置
(3)反应过程中要不断通入CO2,其主要作用是①________,②________.
Ⅱ.探究FeBr2的还原性,
(1)实验需要90 mL 0.1 mol·L-1FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外还需的玻璃仪器是________。
(2)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。
设计实验证明假设2是正确的_______________________________
(3)实验证明:还原性Fe2+>Br-请用一个离子方程式来证明:______________________________;
(4)若在40mL上述FeBr2溶液中通入3×10-3molCl2,则反应的离子方程式为:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应2N2O5(g)═4NO2(g)+O2(g)开始时,c(N2O5)=0.040 8molL﹣1,经1min后,c(N2O5)=0.030 0molL﹣1.则该反应的反应速率为( )
A.v(N2O5)=1.80×10﹣3 molL﹣1min﹣1
B.v(N2O5)=1.08×10﹣2 molL﹣1min﹣1
C.v(NO2)=1.80×10﹣3 molL﹣1min﹣1
D.v(O2)=1.80×10﹣2 molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中表现出的性质是 .
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是 ,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是 mol.
(3)0.3molCu被另一浓度的硝酸完全溶解后,如果此时产生的NO和NO2气体总体积在标准状况下为8.96L,则被还原的硝酸的物质的量是 mol,参加反应的硝酸的物质的量是 mol,产生的混合气体中NO和NO2体积比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列叙述中正确的是
A.用活性炭为榶浆脱色和用双氧水漂白纸浆,其原理相同
B.铜制品在潮湿空气中生锈,其主要原因是发生析氢腐蚀
C.静置后的淘米水能产生丁达尔现象,这种“淘米水”是胶体
D.新型能源生物柴油和矿物油主要化学成分相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:制备溴乙烷的的一种方法是乙醇与氢溴酸反应,该反应的化学方程式为:CH3CH2OH+HBr![]() CH3CH2Br+H2O。
CH3CH2Br+H2O。
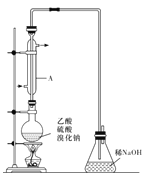
I.实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是 。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 (填写正确选项的字母)。
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
II.溴乙烷的性质实验
(4)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是 。通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液
(5)溴乙烷与NaOH乙醇溶液共热可产生乙烯气体。在进行该实验时,把生成的气体通过右图所示的装置。用该装置进行实验的目的是检验乙烯的生成,该图中右侧试管中的现象是______________;左侧试管中水的作用是___________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他产物已略去):
![]()
(1)若A、D的水溶液均呈酸性,且D为强酸.
①A、D分别为A: ,D: .(填写化学式,下同)
②写出B→C转化的化学方程式: .
③简述检验B物质的方法 .
④写出D的浓溶液和Cu在加热条件的化学方程式 .21*cnjy*com
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.
①工业上合成A的化学方程式: .在实验室中则用加热固体混合物的方法制取气体A,其化学方程式为 .
②写出C→D的化学方程式,并用双线桥标出电子转移的方向和数目.
③写出A→B的化学方程式
④1.92g铜投入一定的D浓溶液中,铜完全溶解,共收集到672mL气体(标准状况).将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为 mL.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com