
| A. | Zn与稀H2SO4反应:Zn+2H+═Zn2++H2↑ | |
| B. | 铁和稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | Cl2与NaOH溶液反应:Cl2+2OH-═2Cl-+H2O | |
| D. | 碳酸钙溶于盐酸:CO32-+2H+═CO2↑+H2O |
分析 A.锌与稀硫酸反应生成硫酸锌和氢气;
B.铁与稀硝酸反应生成NO气体,不会生成氢气;
C.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
D.碳酸钙为难溶物,离子方程式中不能拆开.
解答 解:A.Zn与稀H2SO4反应生成硫酸锌和氢气,反应的离子方程式为:Zn+2H+═Zn2++H2↑,故A正确;
B.铁和稀硝酸反应没有氢气生成,铁过量3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,离子反应为:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,铁少量Fe+4HNO3═Fe(NO3)3+NO↑+2H2O,离子反应为Fe+4H++NO3-═Fe3++NO↑+2H2O,故B错误;
C.Cl2与NaOH溶液反应生成氯化钠、次氯酸钠和水,正确的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故C错误;
D.碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故D错误;
故选A.
点评 本题考查了离子方程式的判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:选择题
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
| A. | 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2) | |
| B. | 平衡时,升高温度,Ⅰ中速率减慢,Ⅱ中速率加快 | |
| C. | 当密度不变时,上述反应即达平衡 | |
| D. | 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉水解的最终产物是葡萄糖 | |
| B. | 重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤 | |
| C. | 盐析可提纯蛋白质并能保持蛋白质的生理活性 | |
| D. | 油脂都不能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35Cl和37Cl的原子核外电子排布不同 | |
| B. | CO2通入Na2SiO3溶液中可以得到硅酸溶胶 | |
| C. | 短周期主族元素原子最外层电子数一定等于其最高化合价 | |
| D. | 1 mol HCl分子和1 mol HF分子断键需要的能量前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
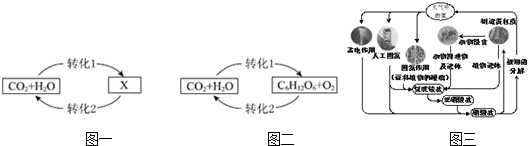
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 二氧化硅溶于NaOH溶液:SiO2+2OH-═SiO32-+H2O | |
| C. | 单质钠放入水中,产生气体:Na+H2O═Na++OH-+H2↑ | |
| D. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com