
【题目】当溶液中有大量的H+和Ba2+时,下列离子中有可能大量存在的是( )
A. SO42- B. CO32- C. Cl- D. OH-
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】化合物M是一种合成药品的中间体,其合成路线如图所示。
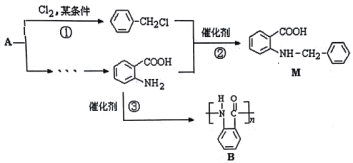
已知: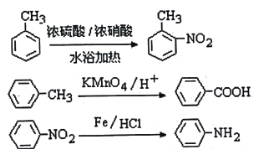
(弱碱性,易被氧化)
(1)写出反应①的化学方程式_____________。
(2)反应②属于____反应(填有机反应类型)。
(3)写出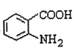 中官能团的名称__________。
中官能团的名称__________。
(4)H为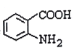 的同分异构体,则满足下列条件的H的同分异构体共有______种,其中满足下列条件且含4种不同氢原子的同分异构体的结构简式是___________。
的同分异构体,则满足下列条件的H的同分异构体共有______种,其中满足下列条件且含4种不同氢原子的同分异构体的结构简式是___________。
①显弱碱性,易被氧化 ②分子内含有苯环 ③能发生水解反应
(5)请你设计由A合成B的合成路线_________________________________________________________。
提示:①合成过程中无机试剂任选; ②合成路线表示方法示例如图所示。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)(题文)在恒温、恒容条件下,能说明可逆反应:H2(g)+I2(g) 2HI(g)达到平衡状态的是
A. 气体的压强保持不变 B. v(H2)正=2v(HI)逆
C. 气体的密度保持不变 D. 气体的颜色保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的5种短周期元素,A最外层电子数是其电子层数的两倍;B能形成双原子阴离子;C与B能形成两种常见的离子化合物,B、E同主族,C、D、E的最高价氧化物对应的水化物之间两两皆能反应生成盐和水。请回答下列问题:
(1)B的双原子阴离子电子式为_______,用化学式表示一种由B、C、E组成的物质_____。
(2)B的氢化物比E的氢化物的沸点____ (填“高”或“低”),理由是__________。
(3)B、C、D组成化合物的水溶液与过量AB2反应的离子方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种溶液A、B各1mL,分别加水稀释到1000mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图示,下列说法正确的是( )
①若 a<4,则A、B都是弱酸
②稀释后,A酸溶液的c(H+ )比B酸溶液c(H+ )大
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等.

A. ①④ B. ②③ C. ①② D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将m1g铜铝合金投入到1 L含H2SO4和HNO3的混合溶液中,合金完全溶解后只生成VL —氧化氮气体(标准状况),向反应后的溶液中逐滴加入1mol/L NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积的关系如下图所示。下列说法中不正确的是:

A. 2c(H2SO4) + c(HNO3) = 0.8 mol·L-1
B. m2—m1=5.1
C. 原合金中铝的质量分数为34.7%
D. V = 2.24
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴被誉为战略物资,有出色的性能和广泛的应用。以水钴矿(主要成分为Co2O3、CoO、CuO、Fe2O3、CaO、MgO、NiO和SiO2等)为原料制备CoCl2·6H2O的工艺流程如图所示:

回答下列问题:
Ⅰ.“酸浸”
(1)钴的浸出率随酸浸时间、温度的变化关系如下图所示。综合考虑成本,应选择的最佳工艺条件为_________、_________;滤渣①的主要成分为__________。

(2)Co2O3与浓硫酸反应生成CoSO4,化学方程式为______________________________。
Ⅱ.“净化除杂”分三步完成:
(3)除铁:加入适量Na2SO4固体,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,离子方程式为____________________________________。
(4)除钙、镁:加入适量NaF,当Mg2+恰好完全被除去(离子浓度等于10-5mol·L-1)时,c(Ca2+)=_____________mol·L-1 (取两位有效数字)。已知:Ksp(MgF2)=7.4×10-11,Ksp(CaF2)=1.5×10-10。
(5)除铜:加入适量Na2S2O3,发生反应2CuSO4+2Na2S2O3+2H2O=Cu2S↓+S↓+2Na2SO4+2H2SO4,该反应的还原产物为___________。
Ⅲ.“萃取和反萃取”
(6)“水相①”中的主要溶质是Na2SO4和________(写化学式)。
(7)实验室称取100g原料(含钴11.80%),反萃取时得到浓度为0.036mol·L-1的CoCl2溶液5L,忽略损耗,钴的产率=______(产率=![]() )。
)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com