
(选考)化学·选修2:化学与技术(15分)水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)水的净化和软化的区别是________。
(2)①生活用水必须保证安全,自来水厂需要对取自江河湖泊中的淡水进行杀菌消毒、混凝沉淀、过滤等工艺处理,这三项处理的正确顺序是_________。
②下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是_______填字母)。
a.福尔马杯 b.漂白粉 c.氯气 d.臭氧
(3)Na2FeO4是一种新型水处理剂,工业上可用FeSO4制备Na2FeO4其工艺流程如下:

①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加人绿矾。请解释这一做法的原因:________________________。(用必要的离子方程式和文字描述)。
②写出由Fe(OH)3制取Na2FeO4的化学方程式:____________。
(4)石灰纯碱法是常用的硬水软化方法,已知25℃时 ,现将等体积的Ca(OH)2溶液与Na2CO3溶液混合(假设溶液体积具有加和性),若Na2CO3溶液的浓度为
,现将等体积的Ca(OH)2溶液与Na2CO3溶液混合(假设溶液体积具有加和性),若Na2CO3溶液的浓度为 ,则生成沉淀所需Ca(OH)2溶液的最小浓度为____________。
,则生成沉淀所需Ca(OH)2溶液的最小浓度为____________。
(1)水的净化是用混凝剂将水中的胶体及悬浮物沉淀下来,而水的软化是除去水中较多的钙离子和镁离子(2分)
(2)①混凝沉淀→过滤→杀菌消毒(2分) ②d(2分)
(3)①Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)3胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-=4Fe(OH)3(胶体)(3分)
②2Fe(OH)3+3NaClO+4NaOH==2Na2FeO4+3NaCl+5H2O(3分)
(4)2.0×10-4 mol·L-1 (3分)
【解析】
试题分析:(1)水的净化是用混凝剂将水中的胶体及悬浮物沉淀下来,而水的软化是除去水中较多的钙离子和镁离子;(2)①生活用水必须保证安全,自来水厂需要对取自江河湖泊中的淡水进行杀菌消毒、混凝沉淀、过滤等工艺处理,这三项处理的正确顺序是混凝沉淀→过滤→杀菌消毒;②下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是臭氧;①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加人绿矾。原因:Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)3胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-=4Fe(OH)3(胶体);②由Fe(OH)3制取Na2FeO4的化学方程式:
2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O;
(4)Ksp(CaCO3)=2.8×10-9=c(Ca2+)·c(CO32-)=c(Ca2+)×5.6×10-5mol/L,c(Ca2+)=2.0×10-4 mol·L-1,则生成沉淀所需Ca(OH)2溶液的最小浓度为2.0×10-4 mol·L-1。
考点:考查氧化还原反应、无机流程题、难溶物的Ksp有关计算。


科目:高中化学 来源:2014-2015甘肃省白银市高二上学期期末化学试卷(解析版) 题型:选择题
已知下列热化学方程式
⑴C(s)+1/2O2(g)=CO(g) △H1=-110. 5kJ/mol
⑵2H2(g)+O2(g)=2H2O(g) △H2=-483.6 kJ·
由此可知 C(s)+ H2O(g) == CO(g) + H2(g) ΔH3 。则 ΔH3等于
A.+131.3kJ·mol-1 B.-131.3kJ·mol-1
C.+373.1kJ·mol-1 D.-373.1kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
据2013年4月6日搜狐网站报道:国家质检总局称,在我国销售的德国NUK牌婴儿爽身粉含有一种致癌物“滑石粉”。己知滑石粉的化学式为Mg3(Si4O10)(OH)2,色白、滑爽、柔软、耐火性。下列有关说法不正确的
A.滑石粉属于无机硅酸盐类物质
B.滑石粉组成可表示为3MgO·4SiO2·H2O
C.爽身粉中添加滑石粉是利用它的滑爽、柔软、耐火性
D.滑石粉可能会与氢氟酸、NaOH溶液发生反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列有关叙述正确的是
A.2.24 L CCl4中含有的原子数为0.3NA
B.0.2mol/L的Fe2(SO4)3溶液中SO42-总数为0.6NA
C.5.6 g铁粉与硝酸完全反应失去的电子数一定为0.3NA
D.28 g N2和CO的混合气体含有的原子总数为2NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省天一高三上学期大联考化学试卷(解析版) 题型:选择题
25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是

A.HA溶液的物质的量浓度为0.0l mol·L—1
B.b→c的过程中,温度降低的原因是溶液中发生了吸热反应
C.a→b的过程中,混合溶液中可能存在:c(A-)=c(Na+)
D.25℃时,HA的电离平衡常数K约为1.43×10—2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省天一高三上学期大联考化学试卷(解析版) 题型:选择题
FeCl3溶液与KSCN溶液混合时存在下列平衡:Fe3+(aq)+SCN-( aq)  Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是
Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是
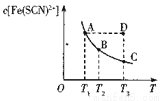
A.该反应为吸热反应
B.T1、T2时反应的平衡常数分别为K1、K2,则K1>K2
C.反应处于D点时,一定有v正大于v逆
D.A点的c(Fe3+)比B点的c(Fe3+)大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邯郸市高三上学期1月教学质量检测化学试卷(解析版) 题型:选择题
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol·L-1的HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.等浓度、等体积的Na2CO3和NaHCO3混合: >
>
C.0.1 mol·L-1 的NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三上学期期末化学试卷(解析版) 题型:选择题
下列事实对应的化学用语正确的是
A.金属钠加入滴有酚酞的水中,溶液变红:Na+ 2H2O=Na+ + 2OH- + H2↑
B.用NaOH溶液吸收多余的氯气:Cl2 + 2OH- =Cl- + ClO-+ H2O
C.将NaHCO3溶液和过量Ca(OH)2溶液混合有白色沉淀:2HCO3-+Ca2++2OH-=CaCO3↓+ 2H2O + CO32-
D.将醋酸溶液滴到大理石上有气泡产生:2H+ + CaCO3=CO2↑+ Ca2+ + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com