
Ī����[(NH4)2Fe(SO4)2��6H2O]����������ԭ�ζ����Ļ����ʣ������йظ�����Һ�ıȽϣ�����ȷ����(����)
A��c(SO )��c(NH )��c(NH )��c(Fe2��)��c(H��)��c(OH��) )��c(Fe2��)��c(H��)��c(OH��) |
B��c(SO )��c(NH )��c(NH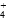 )��c(Fe2��)��c(H��)��c(OH��) )��c(Fe2��)��c(H��)��c(OH��) |
C��2c(SO )��c(OH��)��c(NH )��c(OH��)��c(NH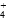 )��2c(Fe2��)��c(H��) )��2c(Fe2��)��c(H��) |
D��c(NH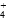 )��c(NH3��H2O)��2c(Fe2��)��2c[Fe(OH)2] )��c(NH3��H2O)��2c(Fe2��)��2c[Fe(OH)2] |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��0.1mol/L��Na2CO3����Һ�У����й�ϵʽ��ȷ����
| A��c(Na+)>c(CO32-)> c(OH��)> c(H+) |
| B��c(OH��)= c(HCO3��)+ c(H2CO3) |
| C��2c(Na+)=c(CO32-)+ c(HCO3��)> c(H2CO3) |
| D��c(Na+)+ c(H+)= c(OH��) + c(HCO3��) +2c(CO32-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
FeCl3��ˮ�ⷽ��ʽ��дΪFeCl3+3H2O 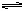 Fe(OH)3+3HCl�������ˮ��̶Ȳ�ȡ�ķ����� ( )
Fe(OH)3+3HCl�������ˮ��̶Ȳ�ȡ�ķ����� ( )
| A�������¶� | B����������Na2CO3 | C�������������� | D������FeCl3��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ڳ����£������й���Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A��1 L 0.1 mol��L��1(NH4)2Fe(SO4)2��6H2O����Һ�У�c( )��c(Fe2��)��c(H��)��c(OH��)��c(
)��c(Fe2��)��c(H��)��c(OH��)��c(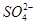 )
)
B��0.1 mol��L��1 NH4HS��Һ�У�c( )��c(HS��)��c(H2S)��c(S2��)
)��c(HS��)��c(H2S)��c(S2��)
C��0.1 mol��L��1 pHΪ4��NaHA��Һ�У�c(HA��)>c(H2A)>c(A2��)
D����Ũ�ȵ�̼���ƺ�̼��������Һ��Ϻ����Һ�У�2c(OH��)��c(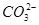 )��c(
)��c( )��3c(H2CO3)��2c(H��)
)��3c(H2CO3)��2c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����ᡢ���ᡢ��������ᶼ��ǿ�ᣬ��������ˮ��Һ�в��������ij�¶������������ڱ������еĵ��볣����
| �� | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6��10��5 | 6.3��10��9 | 1.6��10��9 | 4.2��10��10 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
[˫ѡ��]Ϊ������NH ��Cl��Ũ�ȱ�Ϊ1��1����Һ������NH4Cl��Һ�м���(����)
��Cl��Ũ�ȱ�Ϊ1��1����Һ������NH4Cl��Һ�м���(����)
| A��������HCl | B��ͨ�������� |
| C�������İ�ˮ | D��������NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ˮ�ĵ���ƽ�ⲻ����Ӱ���������(����)
| A��HCl? | B��26M3�� |
C�� | D��CH3COO�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Һ�д��ڵ���ƽ�⣺CH3COOH H����CH3COO��������������ȷ����(����)
H����CH3COO��������������ȷ����(����)
| A��������Һ������Ũ�ȵĹ�ϵ���㣺c(H��)��c(OH��)��c(CH3COO��) |
| B��0.10 mol��L��1��CH3COOH��Һ��ˮϡ�ͣ���Һ��c(OH��)��С |
| C��CH3COOH��Һ�м���������CH3COONa���壬ƽ�������ƶ� |
| D�������£�pH��2��CH3COOH��Һ��pH��12��NaOH��Һ�������Ϻ���Һ��pH<7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��0.102 6 mol��L-1������ζ�25.00 mLδ֪Ũ�ȵ�����������Һ,�ζ����յ�ʱ,�ζ����е�Һ������ͼ��ʾ,��ȷ�Ķ���Ϊ(����)
| A��22.30 mL | B��22.35 mL | C��23.65 mL | D��23.70 mL |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com