
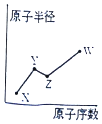
 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | X、Y、Z、W的原子序数递增 | |
| C. | X、W可形成化学式为XW的离子化合物 | |
| D. | 简单离子半径是Z大于W |
分析 X、Y、Z、W是四种常见的短周期元素,Y、Z两种元素的单质是空气的主要成分,Z的原子序数大于Y,可推知Z为O、Y为N,W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N元素,而原子半径小于N原子,故X为H元素,结合元素化合物性质解答.
解答 解:由上述分析可知,X为H,Y为N,Z为O,W为Cl,
A.Y为N,Z为O,二者处于第二周期,W为Cl,处于第三周期,故A错误;
B.X、Y、Z、W的原子序数递增,分别为1、7、8、17,故B正确;
C.X、W可形成化学式为HCl,只含共价键,为共价化合物,故C错误;
D.电子层越多,离子半径越大,则简单离子半径是Z小于W,故D错误;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、原子半径推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧化物:CO2、NO、SO2、H2O | |
| B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | |
| C. | 铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3•H2O | |
| D. | 碱性氧化物:Na2O、CaO、Mn2O7、Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烷烃能使酸性高锰酸钾溶液褪色 | B. | 苯环能使酸性高锰酸钾溶液褪色 | ||
| C. | 甲基使苯环的活性增强 | D. | 苯环使甲基的活性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 种 | B. | 6 种 | C. | 8 种 | D. | 10 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期主族元素W、X、Y、Z的原子序数依次增加.K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一.0.05mol/L丙溶液的pH为1,上述物质的转化关系如图所示.
短周期主族元素W、X、Y、Z的原子序数依次增加.K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一.0.05mol/L丙溶液的pH为1,上述物质的转化关系如图所示.| A. | 丙也可由W、Y组成的某种化合物与K直接反应制得 | |
| B. | K、L、M 中沸点最高的是M | |
| C. | 原子半径:W<X<Y | |
| D. | 元素的非金属性:Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4>SiH4>GeH4>SnH4 | B. | NH3<PH3<AsH3<SbH3 | ||
| C. | H2O>H2S>H2Se>H2Te | D. | HCl<HBr<HI<HF |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t(min) | 2 | 4.5 | 5 | 6 |
| X转化率 | 30% | 40% | 70% | 70% |
| A. | 随着反应的进行,混合气体的密度不断增大 | |
| B. | 反应在5.5min时,v正(X)=v逆(Z) | |
| C. | 6min时,容器中剩余1.4mol Y | |
| D. | 其他条件不变,将X的物质的量改为10mol,则可得4mol Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 恒温恒压容器中,反应A(s)+2B(g)?2C(g)达平衡后,再通入气体C,平衡不移动,气体B的浓度保持不变 | |
| B. | 恒温恒容容器中,通入一定量的N2O4,反应N2O4?2NO2(g)达平衡后,再通入N2O4,平衡正向移动,再达平衡时N2O4的转化率增大 | |
| C. | 恒温下,向密闭容器中加入NH2COONH4固体,反应NH2COONH4(s)?2NH3(g)+CO2(g)达平衡后,缩小容器的容积,再达平衡时,CO2的浓度不变 | |
| D. | 恒温恒容容器中,N2(g)+3H2(g)?2NH3(g)达平恒后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
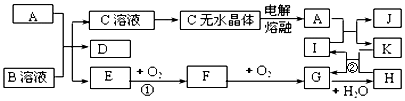
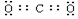 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com