
 燃煤厂为减少SO2的排放,可采取的措施是:
燃煤厂为减少SO2的排放,可采取的措施是:分析 ①二氧化硫使酸性氧化物和碱或碱性盐溶液反应;
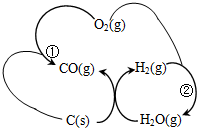
②反应①热化学方程式为:C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5KJ/mol,反应②的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.6KJ/mol,结合盖斯定律和热化学方程式构造所需热化学方程式得到.
解答 解:①洗涤含SO2的烟气,根据酸性氧化物的性质可选,
a.浓NH3?H2O和二氧化硫反应可以吸收二氧化硫,故A正确;
b.NaHCO3 溶液和二氧化硫反应可以吸收二氧化硫气体,故b正确;
c.FeCl3 溶液和二氧化硫发生氧化还原反应,可以吸收二氧化硫,故c正确;
d.NaHSO3不能和二氧化硫发生反应,不能吸收二氧化硫,故d错误;
故答案为:abc;
②反应①热化学方程式为:①C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5KJ/mol,反应②的热化学方程式为:②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.6KJ/mol
依据盖斯定律计算①-②得到C(s)+H2O(g)=CO(g)+H2(g)△H=+131.1 kJ•mol-1,
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.1 kJ•mol-1.
点评 本题考查了物质性质,尾气吸收方法,热化学方程式和盖斯定律的计算应用,掌握基础是解题关键,题目较简单.


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | 平衡不会发生移动 | B. | SO3的质量分数增大 | ||
| C. | 混合气体的密度减小 | D. | 混合气体的平均相对分子质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒的半径:Si>Mg | B. | 氧元素不存在同素异形体 | ||
| C. | Mg的还原性强于Si | D. | 该反应是置换反应,镁元素被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.
苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.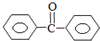 $→_{浓H_{2}SO_{4}、CH_{3}COOH}^{K_{2}S_{2}O_{8}}$
$→_{浓H_{2}SO_{4}、CH_{3}COOH}^{K_{2}S_{2}O_{8}}$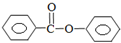
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 血液中溶解的CO2有平衡存在:CO2+H2O?H2CO3?H++HCO3- | |
| B. | 当pH<7.35时造成酸中毒,可静脉滴注NaHCO3溶液解毒 | |
| C. | 病人心肺复苏时大量使用NaHCO3,会造成血液的pH升高,引起碱中毒 | |
| D. | 取一定量pH=8.1的血液稀释到原体积的10倍,pH=7.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L1mol/L的氯化钠溶液中取出10ml后,其浓度仍是1mol/L | |
| B. | NaHSO4溶液与NaOH溶液反应的离子方程式:H++OH-=H2O | |
| C. | FeCl3溶液呈电中性,Fe(OH)3胶体带正电 | |
| D. | 氧化剂具有氧化性,是得到电子(或电子对偏向)的物质,反应时本身被还原 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com