
| A. | 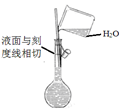 配制溶液 | B. | 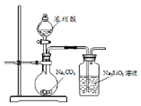 证明非金属性强弱:C>Si | ||
| C. |  除去CO2中的HCl | D. | 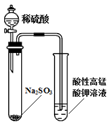 证明SO2有漂白性 |
分析 A.应用胶头滴管定容;
B.盐酸易挥发,生成的二氧化碳中混有HCl;
C.二氧化碳不溶于饱和碳酸氢钠,氯化氢与碳酸氢钠反应生成二氧化碳;
D.二氧化硫和高锰酸钾发生氧化还原反应.
解答 解:A.配制溶液时,为防止溶液加多,应用胶头滴管定容,故A错误;
B.盐酸易挥发,生成的二氧化碳中混有HCl,不能证明碳酸的酸性比硅酸强,则不能证明非金属性强弱:C>Si,故B错误;
C.二氧化碳不溶于饱和碳酸氢钠,氯化氢与碳酸氢钠反应生成二氧化碳,可用于除去HCl,故C正确;
D.二氧化硫具有还原性,与高锰酸钾发生氧化还原反应,如检验二氧化硫的漂白性,应用品红,故D错误.
故选C.
点评 本题考查化学实验方案的评价,涉及溶液的配制、物质的分离等操作,侧重于学生的分析能力、实验能力和评价能力的考查,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 电解后溶液质量减少(m+36)g | |
| B. | 原溶液中Na2SO4的质量分数为$\frac{71m}{161(m+18)}$ | |
| C. | 若其它条件不变,将石墨电极替换为铜电极,则阴极析出2mol H2 | |
| D. | 若其它条件不变,将石墨电极替换为铜电极,则析出Na2SO4•10H2O晶体仍为m g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱溶液和烧碱溶液均呈碱性,说明二者均属于碱 | |
| B. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 | |
| C. | 某酸与Na2CO3反应生成CO2,说明该酸一定是强酸 | |
| D. | 某溶液中滴加KSCN溶液后,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
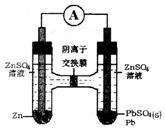
| A. | SO42-从右向左迁移 | |
| B. | 电池的正极反应为:Pb2++2e-═Pb | |
| C. | 左边ZnSO4浓度增大,右边ZnSO4浓度不变 | |
| D. | 若有6.5g锌溶解,有0.1 molSO42-通过离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X、Y的物质的量之比为1:4,且N是黄绿色气体,则该反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | 若M、N为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙色褪色,橙色褪色过程的离子方程式为SO2+Br2+2H2O=4H++SO42-+2Br- | |
| C. | 若X是铁,Y是稀硝酸(过量),则X与Y反应的离子方程式为Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| D. | 当N为氯碱工业的主要原料,M是造成温室效应的主要气体,则上述反应的离子方程式一定为CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论 |
| A | 其他条件不变,缩小H2(g)+I2(g)?2HI(g)的平衡体系的容器容积,气体颜色变深 | 增大压强,平衡逆向移动 |
| B | 分别将乙烯与SO2通入酸性KMnO4溶液中,KMnO4溶液均褪色 | 两种气体使酸性KMnO4溶液褪色的原理不相同 |
| C | 用滴定管量取20.00mL稀硫酸,初读数时尖嘴管内有气泡,末读数时气泡消失 | 所取稀硫酸体积小于20.00mL |
| D | 25℃时,分别测定等物质的量浓度的NaCN溶液和NaF溶液的pH,前者pH大 | 酸性:HCN>HF |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13g乙炔中含有共用电子对的数目为1.5NA | |
| B. | 含有2NA个氧原子的氧气和臭氧的混合气体的质量为32g | |
| C. | 1 mol•L-1碳酸钠溶液中含有的碳酸根离子的数目小于NA | |
| D. | 标准状况下,将22.4LCl2通入水中发生反应,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | 1076 | 465 | x |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com