
【题目】铁、镍及其化合物在工业上有广泛的应用。从某矿渣 ![]() 成分为
成分为![]() 铁酸镍
铁酸镍![]() 、NiO、FeO、CaO、
、NiO、FeO、CaO、![]() 等
等![]() 中回收
中回收![]() 的工艺流程如下:
的工艺流程如下:
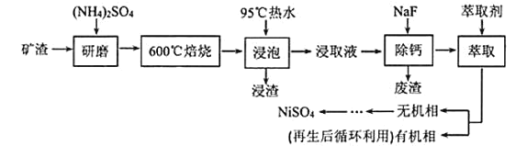
已知![]() 在
在![]() 分解生成
分解生成![]() 和
和![]() ,回答下列问题:
,回答下列问题:
![]() “浸渣”的成分有
“浸渣”的成分有![]() 、
、![]() 、
、![]() 外,还含有_________
外,还含有_________![]() 写化学式
写化学式![]() 。
。
![]() 矿渣中部分FeO焙烧时与
矿渣中部分FeO焙烧时与![]() 反应生成
反应生成![]() 的化学方程式为_____________。
的化学方程式为_____________。
![]() 溶剂萃取可用于对溶液中的金属离子进行富集与分离:
溶剂萃取可用于对溶液中的金属离子进行富集与分离:![]() 水相
水相![]() 有机相
有机相![]() 有机相
有机相![]() 水相
水相![]() 。萃取剂与溶液的体积比
。萃取剂与溶液的体积比![]() 对溶液中
对溶液中![]() 、
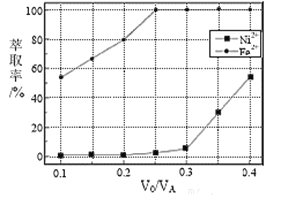
、![]() 的萃取率影响如下图所示,
的萃取率影响如下图所示,![]() 的最佳取值为________。在_______
的最佳取值为________。在_______![]() 填“强碱性”“强酸性”或“中性”
填“强碱性”“强酸性”或“中性”![]() 介质中“反萃取”能使有机相再生而循环利用。
介质中“反萃取”能使有机相再生而循环利用。
![]() 以Fe、Ni为电极制取
以Fe、Ni为电极制取![]() 的原理如下图所示。通电后,在铁电极附近生成紫红色的
的原理如下图所示。通电后,在铁电极附近生成紫红色的![]() ,若pH过高,铁电极区会产生红褐色物质。
,若pH过高,铁电极区会产生红褐色物质。
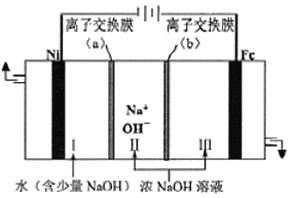
![]() 电解时阳极的电极反应式为_________,离子交换膜
电解时阳极的电极反应式为_________,离子交换膜![]() 为________
为________![]() 填“阴”或“阳
填“阴”或“阳![]() 离子交换膜。
离子交换膜。
![]() 向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为__________。
向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为__________。
【答案】![]()
![]()
![]() 强酸性
强酸性 ![]() 阴
阴 ![]()
【解析】
某矿渣的主要成分是![]() 铁酸镍
铁酸镍![]() 、NiO、FeO、CaO、
、NiO、FeO、CaO、![]() 等,加入硫酸铵研磨后,
等,加入硫酸铵研磨后,![]() 焙烧,已知:
焙烧,已知:![]() 在
在![]() 以上会分解生成
以上会分解生成![]() 和
和![]() 在焙烧过程中生成
在焙烧过程中生成![]() 、
、![]() ,在
,在![]() 的热水中浸泡过滤得到浸出液,加入NaF除去钙离子,过滤得到滤液加入萃取剂得到无机相和有机相,无机相通过一系列操作得到硫酸镍,有机相循环使用,以此解答该题。
的热水中浸泡过滤得到浸出液,加入NaF除去钙离子,过滤得到滤液加入萃取剂得到无机相和有机相,无机相通过一系列操作得到硫酸镍,有机相循环使用,以此解答该题。
根据上述分析可知:
![]() “浸渣”的成分有
“浸渣”的成分有![]() 、
、![]() 、
、![]() 外,还含有
外,还含有 ![]() ;
;
故答案为:![]() ;
;
![]() 矿渣中部分FeO焙烧时与
矿渣中部分FeO焙烧时与![]() 反应生成
反应生成![]() 的化学方程式为
的化学方程式为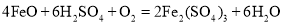 ;
;
故答案为:![]() ;
;
![]() 本工艺中,萃取剂与溶液的体积比
本工艺中,萃取剂与溶液的体积比![]() 对溶液中
对溶液中![]() 、
、![]() 的萃取率影响如图所示,最佳取值是亚铁离子能被萃取,镍离子不被萃取,
的萃取率影响如图所示,最佳取值是亚铁离子能被萃取,镍离子不被萃取,![]() 的最佳取值是
的最佳取值是![]() ,由
,由![]() 水相
水相![]() 有机相
有机相![]() 有机相
有机相![]() 水相
水相![]() 可知,应在强酸性介质中“反萃取”能使有机相再生而循环利用;
可知,应在强酸性介质中“反萃取”能使有机相再生而循环利用;
故答案为:![]() ;强酸性;
;强酸性;
![]() 电解池中阳极发生氧化反应,依据题意可知铁在阳极失去电子,碱性环境下生成高铁酸根离子,电极反应式为:
电解池中阳极发生氧化反应,依据题意可知铁在阳极失去电子,碱性环境下生成高铁酸根离子,电极反应式为:![]() ;离子交换膜
;离子交换膜![]() 为阴离子交换膜,可使氢氧根离子进入阳极区;
为阴离子交换膜,可使氢氧根离子进入阳极区;
故答案为:![]() ;阴;
;阴;
![]() 向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解,该反应的离子方程式为:
向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解,该反应的离子方程式为:![]() ;
;
故答案为:![]() 。
。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】含氮化合物在生产、生命活动中有重要的作用。回答下列问题:
(1)已知4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H1=-alkJ/mol,4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H2=-bkJ/mol,H2O(1)=H2O(g)△H3=+ckJ/mol,写出在298K时,氨气燃烧生成N2的热化学方程式___________。
(2)肌肉中的肌红蛋白(Mb)可与O2结合生成MbO2:Mb(aq)+O2(g)![]() MbO2(aq),其中k正和k逆分别表示正反应和逆反应的速率常数,即V正=k正·c(Mb)·P(O2),V逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]:
MbO2(aq),其中k正和k逆分别表示正反应和逆反应的速率常数,即V正=k正·c(Mb)·P(O2),V逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]:
P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
α(MbO2%) | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
①计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=___________。
②导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=___________(用含有k正、k逆的式子表示)。
(3)构成肌红蛋白的甘氨酸(NH2CH2COOH)是一种两性物质,在溶液中以三种离子形式存在,其转化关系如下:
![]()
![]()
![]()
![]()
![]()
在甘氨酸溶液中加入酸或碱,三种离子的百分含量与![]() 的关系如图所示:
的关系如图所示:

①纯甘氨酸溶液呈___________性;当溶液呈中性时三种离子的浓度由大到小的顺序为___________。
②向![]() =8的溶液中加入过量HCl时,反应的离子方程式为___________。
=8的溶液中加入过量HCl时,反应的离子方程式为___________。
③用电位滴定法可测定某甘氨酸样品的纯度.
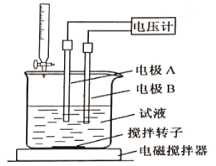
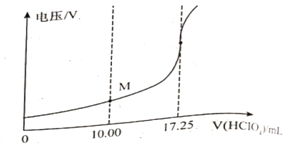
称取样品150mg,在一定条件下,用0.1000mol/L的高氯酸溶液滴定(与甘氨酸1︰1发生反应),测得电压变化与滴入HClO4溶液的体积关系如下图。做空白对照实验,消耗HClO4溶液的体积为0.25mL,该样品的纯度为___________%(计算结果保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2H2(g)+O2(g) ![]() 2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g)
2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq)
2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq) ![]() H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
A. CH3OH的燃烧热为1452 kJ·mol-1
B. 2H2(g)+O2(g) ![]() 2H2O(g) H > -571.6 kJ·mol-1
2H2O(g) H > -571.6 kJ·mol-1
C. CH3COOH(aq)+NaOH(aq) ![]() H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
D. 2CH3OH(l)+O2(g) ![]() 2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用来减轻感冒症状的布洛芬的结构简式如图所示,下列有关说法不正确的是( )
![]()
A.1mol布洛芬能与足量NaHCO3溶液反应最多生成1molCO2
B.布洛芬的分子式为C13H18O2
C.布洛芬苯环上的一溴代物有2种
D.布洛芬与苯甲酸甲酯是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列有机反应类型的认识中,错误的是
A. ![]() ;取代反应
;取代反应
B. CH2=CH2 + Br2![]() CH2Br-CH2Br;加成反应
CH2Br-CH2Br;加成反应
C. 2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O;取代反应
2CH3CHO+2H2O;取代反应
D. CH3COOH + CH3CH2OH ![]() CH3COOCH2CH3+H2O;取代反应
CH3COOCH2CH3+H2O;取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发射嫦娥三号的长征三号乙运载火箭,其中第3级火箭中的能源物质为液态H2和液态O2,发生的反应为2H2(g)+O2(g)===2H2O(g)。下列说法不正确的是( )
A. 化合反应都是放热反应
B. 2 mol气态H2与1 mol气态O2的总能量大于2 mol水蒸气的总能量
C. 断裂2 mol H—H键、1 mol O—O键吸收的总能量小于形成4 mol H—O键释放的总能量
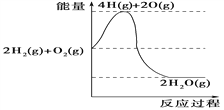
D. 氢气燃烧过程中能量变化可用如图表示:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲同学设计的证明CO具有还原性的实验装置。回答下列问题:
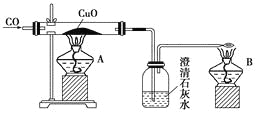
(1)实验时应先点燃________(填“A”或“B”)处的酒精灯。
(2)洗气瓶中的现象为__________________________________________________________。
(3)酒精灯B的作用是_________________________________________________________。
(4)乙同学提出甲设计太复杂,可将酒精灯合二为一,去掉B而将尾气导管口旋转到A的火焰上即可,乙同学设计是否合理?________;理由是______________________________。
(5)丙同学质疑CO能否使石灰水变浑浊,因此其设计在CO通入CuO之前应先通过澄清石灰水以排除CO与澄清石灰水反应,试对此做出评价,你认为丙的设计________(填“必要”或“不必要”),理由是____________________________________________。
(6)丁同学认为甲设计的装置中尾气处理还可以用其他方法,请你为丁同学设计一种合理的尾气处理方法:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol/L CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。

下列说法中正确的是
A.a点表示溶液中c(CH3COO-)约为10-3mol/L
B.b点表示的溶液中c(Na+)>c(CH3COO-)
C.c点表示CH3COOH和NaOH恰好反应完全
D.d点表示的溶液中 大于K
大于K
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com