
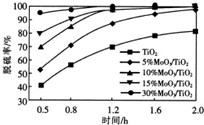
 用TiO2负载MoO3催化剂使有机物R催化脱硫,负载MoO3的量对反应脱硫率的影响如图.下列说法正确的是( )
用TiO2负载MoO3催化剂使有机物R催化脱硫,负载MoO3的量对反应脱硫率的影响如图.下列说法正确的是( )| A. | 负载MoO3的量越大,平衡常数越大 | |
| B. | 当反应时间小于0.5h,脱硫率为0 | |
| C. | 1.6h负载MoO3的量为10%和15%的脱硫率相等 | |
| D. | 0.5~1.2h时,负载MoO3的量越大,脱硫速率越大 |
分析 A、根据平衡常数仅与温度有关判断;
B、根据图象分析,当反应时间小于0.5h,反应仍然在进行;
C、根据图象分析,以1.6h作垂线,分析负载MoO3的量为10%和15%的脱硫率的纵坐标大小;
D、根据图象分析,0.5~1.2h时内任一点作垂线,依据负载MoO3的量的变化分析纵坐标脱硫速率的变化.
解答 解:A、根据平衡常数仅与温度有关,所以负载MoO3的量越大,平衡常数不变,故A错误;
B、根据图象,当反应时间小于0.5h,反应仍然在进行,脱硫率较小,但不等于0,故B错误;
C、根据图象,以1.6h作垂线,负载MoO3的量为10%和15%的脱硫率相等,故C正确;
D、根据图象,0.5~1.2h时内任一点作垂线,负载MoO3的量越大,脱硫率也越大,但是斜率越小,则脱硫速率越小,故D错误;
故选C.
点评 本题考查学生的识图能力,要求学生具有分析和解决问题的能力,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | ① | ② | ③ | ④ |
| pH | 10 | 10 | 4 | 4 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
| A. | 相同体积③、④溶液分别与NaOH完全反应,消耗NaOH物质的量:③>④ | |
| B. | 分别加水稀释10倍,四种溶液的pH①>②>④>③ | |
| C. | ①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | Va L ④溶液与Vb L ②溶液混合(近似认为混合溶液体积=Va+Vb),若混合后溶液pH=5,则Va :Vb=11:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,E、H中所含官能团的名称分别是羟基、碳碳双键.
,E、H中所含官能团的名称分别是羟基、碳碳双键. +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O、n
+H2O、n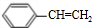 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$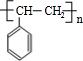 .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
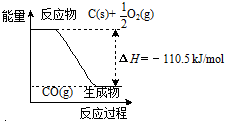
| A. | 12gC(s)与一定量O2(g)反应生成14g CO(g),放出的热量为110.5kJ | |
| B. | 该反应的反应热等于CO分子中化学键形成时所释放的总能量与O2分子中化学键断裂时所吸收的总能量的差 | |
| C. | 该反应的热化学方程式是2C(s)+O2(g)=2CO(g)△H=-221kJ | |
| D. | 2molC(s)与足量O2(g)反应生成CO2(g),放出的热量大于221kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com