
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
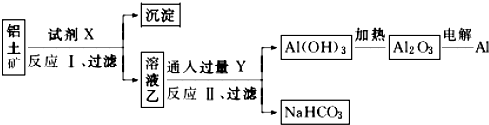
分析 依据工艺流程可知:溶液乙通入过量的Y生成氢氧化铝沉淀、碳酸氢钠,说明溶液中含有偏铝酸钠,气体Y为二氧化碳,则X为强碱,不能是硫酸,溶液乙为偏铝酸盐,氢氧化铝受热分解生成氧化铝,电解氧化铝生成铝,据此解答.
解答 解:①依据工艺流程可知:溶液乙通入过量的Y生成氢氧化铝沉淀、碳酸氢钠,说明溶液中含有偏铝酸钠,气体Y为二氧化碳,则X为强碱,不能是硫酸,故错误;
②过量的二氧化碳与偏铝酸钠反应生成氢氧化铝沉淀与碳酸氢钠,反应方程式为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,离子方程式为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-,故正确;
③结合质子的能力就是指碱性,结合质子能力越强,相应的酸放出质子的能力就越弱,其对应的酸的酸性就越弱,显然酸性强弱HCO3->Al(OH)3>H2O,碱性:OH->AlO2->CO32-,所以结合质子能力:OH->AlO2->CO32-,故正确;
④氯化铝是分子晶体,熔融时不存在铝离子,故错误;
故选:B.
点评 本题为流程题,考查了工业制铝,明确工艺流程和相关物质的性质是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO | B. | Fe2O3 | C. | FeCl3 | D. | Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4.5g SiO2晶体中含有的硅氧键的数目为0.3NA | |
| B. | 向FeI2溶液中通入适量C12,当有1mol1Fe2+被氧化时,共转移的电子的数目为3NA | |
| C. | 12g石墨烯(单层石墨)中含有六元环的个数为0.5NA | |
| D. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戍醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验剩余的药品不能放回原试剂瓶 | |
| B. | 气体实验装置在实验前进行气密性检查 | |
| C. | 滴管不能交叉使用 | |
| D. | 如果少量酒精失火燃烧,可用湿抹布盖灭火焰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com