
与c(H+)·c(OH-)=Kw类似,FeS饱和溶液中存在:FeS(s) Fe2+(aq)+S2-(aq),
Fe2+(aq)+S2-(aq),
c(Fe2+)·c(S2-)=Ksp。常温下Ksp=8.1×10-17。
(1)理论上FeS的溶解度为____________________________________________。
(2)又知FeS饱和溶液中c(H+)与c(S2-)之间存在以下限量关系:[c(H+)]2·c(S2-)=1.0×10-22,为了使溶液中c(Fe2+)达到1 mol/L,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)为______。
:(1)7.92×10-8 g (2)1.11×10-3 mol·L-1
【解析】(1)由FeS(s) Fe2+(aq)+S2-(aq)
Fe2+(aq)+S2-(aq)
c(Fe2+)=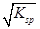 =
=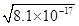 =9×10-9
mol·L-1
=9×10-9
mol·L-1
即1 L溶液中可溶解9×10-9 mol的FeS(令所得溶液的密度为1 g·cm-3)
由(100 g+S)∶S=1 000 g∶(9×10-9×88)g
所以S=7.92×10-8 g
(2)c(Fe2+)=1 mol·L-1,则c(S2-)=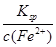 =
=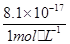 =8.1×10-17mol·L-1,c(H+)=
=8.1×10-17mol·L-1,c(H+)=
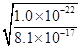 =1.11×10-3 mol·L-1。
=1.11×10-3 mol·L-1。
考点:难容电解质溶解平衡的应用,及简单计算
点评:计算题是高中学生一大难题,平时要注意计算能力的训练以及书写的规范。


 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 键能 | 键能 | 键能 | 键能 | ||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | H-O | 464 |
| S=S | 255 | H-S | 339 | C-F | 427 | C-O | 347 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 W是某短周期元素X的固态单质,A、B、C均为含X元素的酸式钠盐,它们在一定条件下有如图所示的转化关系,其中某些反应产物中的
W是某短周期元素X的固态单质,A、B、C均为含X元素的酸式钠盐,它们在一定条件下有如图所示的转化关系,其中某些反应产物中的

| 7 |
| 4 |
| 7 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物在反应中,常有原子间的共价键全部或部分断裂,如C—H、C—C、C=C、
C—O、C=O等。下列各反应中,反应物分子中断裂键的排列,正确的组合是
| 化学反应 | 乙醇酯化 | 乙醇与钠 | 乙醛氧化 | 乙醛加氢 |
| A | O—H | C—H | C—H | C—O |
| B | O—H | O—H | C—H | C=O |
| C | C—O | C—O | C—H | C=O |
| D | C—O | C—H | C—C | C—O |
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物在反应中,常有原子间的共价键全部或部分断裂,如C—H、C—C、C=C、C—O、C=O等。下列各反应中,反应物分子中断裂键的排列,正确的组合是
| 化学反应 | 乙醇酯化 | 乙醇与钠 | 乙醛氧化 | 乙醛加氢 |
| A | O—H | C—H | C—H | C—O |
| B | O—H | O—H | C—H | C=O |
| C | C—O | C—O | C—H | C=O |
| D | C—O | C—H | C—C | C—O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com